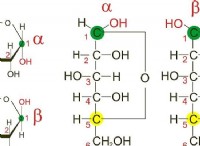
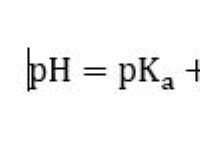pH 및 히드로 늄 이온 이해
* pH : 용액의 산도 또는 알칼리도 측정. 그것은 히드로 늄 이온의 농도 (H₃O⁺)에 기초합니다.
* 히드로 늄 이온 (h₃o⁺) : 산으로부터의 수소 이온 (H⁺)이 물 분자 (H₂O)와 결합 될 때 형성된다.
관계
pH 척도는 로그이며, 이는 pH의 각 수 변화가 하이드로 늄 이온 농도의 10 배 변화를 나타낸다는 것을 의미한다. 히드로 늄 농도를 계산하기위한 공식은 다음과 같습니다.
[h⁻o =] =10ph
계산
1. pH 값을 대체하십시오 : [h⁻o =] =10 ³⁰
2. 계산 : [h 0.o =] =0.001 m (어금니)
답 :
pH 3.0에서 산성 비의 히드로늄 농도는 0.001m (또는 1 x 10 ³ m)이다.