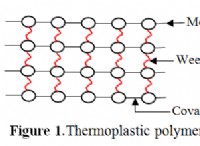
혼성화 및 시그마 본드 이해
* 혼성화 : 원자 궤도를 결합하여 결합에 적합한 새로운 하이브리드 궤도를 형성하는 과정.
* 시그마 (σ) 본드 : 핵 축을 따라 원자 궤도의 직접 겹침에 의해 형성된 가장 강력한 유형의 공유 결합.
분자 분석
1. CH4 (메탄) : 메탄의 탄소에는 4 개의 단일 결합이 있습니다. 즉, Sp³ Hybridized입니다. 모든 채권은 Sp³sp³ Sigma Bonds입니다.
2. C2H6 (에탄) : 에탄의 각 탄소에는 4 개의 단일 결합 (1 대의 탄소, 3 개는 수소)이 있습니다. 그것들은 sp³ 혼성화되어 Sp³sp³ sigma bonds를 초래합니다.
3. C2H4 (Ethene) : Ethene의 각 탄소에는 3 개의 Sigma 결합 (1 대의 탄소, 2 개는 수소 2 개) 및 1 개의 PI 결합이 있습니다. 이것은 각 탄소 원자에 대한 SP² 하이브리드 화를 나타냅니다. 따라서, C-C 결합은 sp²sp² 시그마 본드 이다 .
4. C2H2 (Ethyne) : Ethyne의 각 탄소에는 2 개의 Sigma 결합 (하나는 다른 탄소와 하나는 수소)과 2 개의 PI 결합이 있습니다. 이것은 각 탄소 원자에 대한 SP 혼성화를 나타냅니다. C-C 결합은 spsp sigma bond 입니다 .
결론
sp²sp² sigma bond를 함유하는 분자는 c2h4 (ethene) 입니다. .