순수한 물질
* 입자는 모두 동일합니다. 순수한 물질은 한 가지 유형의 입자로 만 구성됩니다. 동일한 대리석 상자처럼 생각하십시오.
* 고정 구성 : 입자의 비율은 샘플을 어디에서 가져 가든 항상 동일합니다.
* 특정 특성 : 순수한 물질에는 독특한 용융 및 끓는점, 밀도 및 기타 속성이 변하지 않는 특성이 있습니다.
예 :
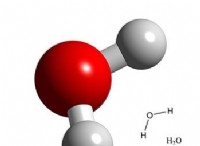
* 물 (h>o) : 고정 된 비율의 수소와 산소 입자로만 만들어졌습니다.
* 금 (Au) : 금 원자로 만 구성됩니다.
* 설탕 (c>h₂₂o₁₁) : 설탕 분자로 만 구성됩니다.
혼합물
* 입자는 다릅니다 : 혼합물은 둘 이상의 다른 유형의 입자로 구성됩니다. 색상과 크기가 다른 대리석 상자를 상상해보십시오.
* 가변 조성 : 다른 입자의 비율은 다를 수 있습니다. 당신은 다른 유형의 입자보다 더 많은 유형의 입자와 혼합물을 가질 수 있습니다.
* 고정 속성 없음 : 혼합물은 다양한 용융점, 끓는점 및 밀도를 가질 수 있습니다.
예 :
* 바닷물 : 염 (NaCl) 입자 및 물 (HATE) 입자의 혼합물.
* 공기 : 질소, 산소, 이산화탄소 및 기타 가스의 혼합물.
* 모래와 물 : 모래 입자와 물 입자의 혼합물.
키 포인트 : 입자 이론은 배열 및 유형을 강조합니다 입자의 순수한 물질과 혼합물의 차이를 이해하는 데 중요합니다.