1. 주요 개념을 이해하십시오
* 농도 : 주어진 양의 용매 또는 용액에 용해 된 용질의 양을 설명합니다. 공통 단위는 다음과 같습니다.
* Molarity (m) : 용액 리터당 용질의 두부 (mol/L)
* 질량 퍼센트 (% w/w) : 용액 100 그램 당 용질 그램
* 1 백만 분당 부품 (ppm) : 용액 1 리터당 용액 밀리그램 (mg/l)
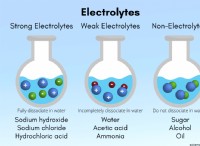
* 용질 : 용해되는 물질 (예 :물에 소금).
* 용매 : 용해를 수행하는 물질 (예 :물).
* 솔루션 : 용질 및 용매에 의해 형성된 균질 혼합물.
2. 공식
용액에서 화합물의 그램을 계산하는 기본 공식은 주어진 농도 단위에 따라 다릅니다.
* Molarity (m) :
* Grams =(Molarity x Volume (l) x Molar Mass (g/mol))
* 질량 퍼센트 (% w/w) :
* Grams =(질량 / 100) x 용액의 질량 (g)
* 1 백만 분당 부품 (ppm) :
* 그램 =(ppm x 볼륨 (l) x 10^-6) (PPM은 MG/L이므로 그램으로 변환해야합니다)
3. 예제 계산
예 1 :Molarity 사용
* 0.50m NaCl 용액 250ml가 있습니다. NaCl의 질량은 무엇입니까?
* 1 단계 : 부피를 리터로 변환하십시오 :250 ml =0.25 l
* 2 단계 : NaCl의 몰 질량은 58.44 g/mol입니다.
* 3 단계 : 공식을 적용하십시오.
* 그램 =(0.50 mol/l * 0.25 l * 58.44 g/mol) = 7.31 그램 naCl
예 2 :질량 퍼센트 사용
* 500 그램의 10% (w/w) 설탕 용액이 있습니다. 몇 그램의 설탕이 존재합니까?
* 1 단계 : 공식을 적용하십시오.
* 그램 =(10 / 100) * 500 그램 = 설탕 50 그램
예 3 :백만마다 부품 사용 (ppm)
* 물 샘플의 납 농도는 15 ppm입니다. 1 리터의 물에서 납 질량은 얼마입니까?
* 1 단계 : 공식을 적용하십시오.
* 그램 =(15 ppm * 1 l * 10^-6) = 0.015 납
4. 중요한 메모
* 공식을 적용하기 전에 항상 단위가 일관성이 있는지 확인하십시오.
* 솔루션의 질량이 주어지면 솔루션의 밀도를 사용하여 볼륨을 계산할 수 있습니다.
* 여러 용질이있는 솔루션으로 작업하는 경우 각 용질의 농도를 개별적으로 알아야합니다.
특정 계산을 염두에두고 계산을 안내 할 수 있다면 알려주십시오.