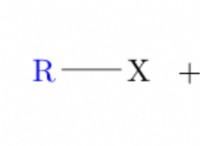1. 전해질 : 바닷물은 우수한 전해질이므로 전기를 전달합니다. 이것은 부식을 유발하는 전기 화학 반응에 중요합니다. 철이 바닷물과 접촉하면 양극으로 작용하여 전자를 잃고 철 이온을 형성합니다 (Fe²⁺). 이 이온은 바닷물에 용해됩니다.
2. 산소 : 바닷물에는 용존 산소가 풍부합니다. 산소는 부식 공정에서 음극으로 작용하여 전자를 받아들이고 수산화물 이온을 형성합니다 (OH⁻). 이 과정은 부식을 더욱 가속화합니다.
3. 클로라이드 이온 : 바닷물에는 클로라이드 이온 (Cl⁻)이 포함되어 있습니다. 이 이온은 부식을 가속화하는 데 중요한 역할을합니다.
* 탈분극 : 클로라이드 이온은 철 이온과 반응하여 가용성 염화물 화합물을 형성합니다. 이 과정은 표면에서 철 이온을 제거하여 부식이 계속 될 수 있습니다.
* 파괴 패권 : 철은 일반적으로 추가 부식 (패시베이션)에 저항하는 얇은 보호 산화 층을 형성합니다. 클로라이드 이온은이 보호 층을 분해하여 철분이 부식에 더 취약하게 만듭니다.
4. 가속 반응 : 바닷물에 산소와 클로라이드 이온의 존재는 부식 과정을 상당히 가속화시킨다. 이는 부식으로 이어지는 전기 화학적 반응이 양극과 음극 반응이 촉진되는 환경에서 훨씬 더 빠르게 진행하기 때문입니다.
요약 : 바닷물은 전도도, 산소 함량, 염화물 이온 및 결과적으로 가속화 된 전기 화학 반응으로 인해 철의 빠른 부식을위한 완벽한 환경을 제공합니다.