다른 유형의 물질의 화학적 특성
화학적 특성은 물질이 다른 물질과 어떻게 반응하는지 또는 조성을 변화시키는 방법을 설명합니다. 그것들은 물리적 특성과 구별되며, 화학적 화장을 변경하지 않고 물질의 외관, 상태 또는 행동을 설명합니다.
다음은 다양한 유형의 물질에 대한 화학적 특성의 고장입니다.
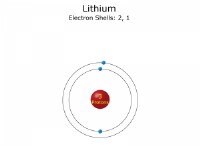
1. 요소 :
* 반응성 : 요소가 다른 요소와 결합하여 화합물을 형성하는 방법.
* 예 :나트륨은 물과 매우 반응하지만 금은 상대적으로 반응하지 않습니다.
* 산화 상태 : 전하 요소는 일반적으로 화합물을 형성 할 때 가정합니다.
* 예 :산소는 일반적으로 대부분의 화합물에서 -2의 산화 상태를 갖습니다.
* 연소 : 산소가있을 때 요소가 연소되는지 여부.
* 예 :탄소는 석탄과 목재의 형태로 쉽게 연소됩니다.
* 부식 : 환경과의 화학적 반응으로 요소가 손상되거나 약화되는 경향.
* 예 :산소와 물에 노출 될 때 철사가 있습니다.
2. 화합물 :
* 산도/염기성 : 화합물은 양성자 (H+ 이온)를 기증하거나 수용하는 능력에 따라 산성, 기본 또는 중성 일 수 있습니다.
* 예 :염산 (HCL)은 산성이고 수산화 나트륨 (NaOH)은 기본입니다.
* 용해도 : 용매 (일반적으로 물)에 용해되는 화합물의 능력.
* 예 :설탕은 물에 용해되지만 기름은 그렇지 않습니다.
* 가연성 : 산소의 존재하에 화합물이 연소되는 능력.
* 예 :메탄 (CH4)은 가연성이 높고 소금 (NaCl)은 그렇지 않습니다.
* 분해 : 화합물이 특정 조건 하에서 더 간단한 물질로 분해되는 경향.
* 예 :과산화수소 (H2O2)는 물 (H2O) 및 산소 (O2)로 분해됩니다.
3. 혼합물 :
* 성분 간의 화학 반응 : 혼합물의 성분은 서로 반응하여 새로운 화합물로 이어질 수 있습니다.
* 예 :철 파일과 황의 혼합물에서 가열은 화학 반응을 일으켜 황화철을 형성 할 수 있습니다.
* 분리 기술 : 혼합물은 성분의 다른 화학적 특성에 따라 분리 될 수 있습니다.
* 예 :증류는 끓는점에 따라 혼합물을 분리하는 데 사용됩니다.
키 포인트 :
* 화학적 특성은 고유 입니다 물질로, 그것을 식별하고 특성화하는 데 사용될 수 있습니다.
* 화학적 특성은 종종 물질 내에서 원자의 배열 및 결합에 의해 결정됩니다. .
* 화학적 특성은 화학 반응에 의해 변경 될 수 있습니다 , 이로 인해 특성이 다른 새로운 물질이 형성됩니다.
일상 생활에서 화학적 특성의 예 :
* 음식 부패 : 음식이 부패하게하는 화학 반응은 화학적 특성의 결과입니다.
* 금속 녹슬 : 이것은 철, 산소 및 물 사이의 화학 반응입니다.
* 연소 : 불타는 목재 또는 가스는 산소와 연료와 관련된 화학 반응입니다.
화학적 특성을 이해하는 것은 화학, 생물학, 의학 및 공학과 같은 다양한 분야에서 중요합니다. 이를 통해 물질이 어떻게 행동하고, 새로운 재료를 설계하고, 새로운 기술을 개발하는지 예측할 수 있습니다.