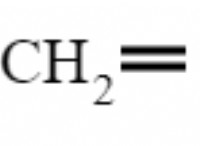* 질소의 전자 구성 : 질소에는 5 개의 원자가 전자가 있습니다. 안정적인 옥셋 (외부 쉘에 8 개의 전자)을 달성하려면 3 개가 더 필요합니다.
* 공유는 돌보고 있습니다 : 다른 질소 원자와 전자를 공유하면 두 원자가 모두 낙지를 완성 할 수 있습니다.
* 강한 트리플 본드 : 3 개의 공유 전자 쌍은 강력하고 짧은 트리플 본드를 만듭니다. 그렇기 때문에 N₂ 분자가 안정적이고 결합 에너지가 높은 이유입니다.
여기에 고장이 있습니다 :
1. 각 질소 원자는 3 개의 원자가 전자를 결합에 기여합니다. .
2. 6 개의 공유 전자는 3 쌍을 형성하여 트리플 본드 (N≡N)를 형성합니다.
3. 이 배열은 외부 껍질에있는 각 질소 원자 8 8 전자를 제공합니다 (공유 전자에서 자체 비 결합 쌍 + 6에서 2). .
이 트리플 결합은 질소 가스가 원소 형태로 너무 반응하지 않는 이유입니다. 그 강한 유대를 깨는 데는 많은 에너지가 필요합니다.