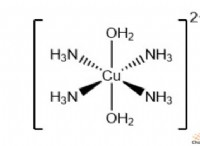
pH =-log₁₀ [h⁺]
어디:
* pH 수소의 잠재력, 용액의 산도 또는 알칼리도의 척도에 대한 상징입니다.
* 로그 베이스 -10 로그입니다.
* [h [] 용액에서 수소 이온 (H⁺)의 몰 농도를 나타냅니다.
설명 :
pH 스케일은 0에서 14 사이의 로그 스케일이며, 7 인 용액은 중립으로 간주된다. 7 미만의 pH를 갖는 용액은 산성이며, pH가 7보다 큰 용액은 기본이다 (알칼리).
공식은 pH가 수소 이온의 농도에 반비례한다는 것을 보여준다. 이는 더 높은 농도의 수소 이온이 더 낮은 pH (더 산성)를 초래하고, 더 낮은 농도의 수소 이온이 더 높은 pH (더 염기성)를 초래한다는 것을 의미한다.
예 :
용액에서 수소 이온의 농도가 1 x 10 ℃ 인 경우, 용액의 pH는 다음과 같이 계산 될 수있다.
```
pH =-log₁₀ [H⁺]
pH =-log₁₀ (1 x 10⁻⁵)
pH =5
```
이것은 용액이 산성임을 나타냅니다.





![은하수의 가장 밝은 별 패치 이미지 [환상적인 천체]](/article/uploadfiles/202211/2022111014564884_S.jpg)