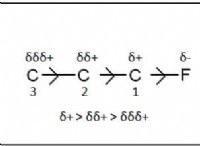
이유는 다음과 같습니다.
* 산도 및 알칼리도는 ph. 에 의해 정의됩니다 pH는 용액에서 수소 이온 (H+)의 농도의 척도이다.
* 산성 용액은 농도의 H+ 이온 농도를 가지므로 pH가 낮아 (일반적으로 7 미만)
* 알칼리성 (기본) 용액은 H+ 이온의 농도가 낮아서 pH가 더 높아서 (일반적으로 7 이상)
* 중성 용액의 pH는 7입니다. 이것은 H+ 및 OH 이온 (수산화물 이온)의 농도가 동일합니다.
따라서 물질은 pH에 따라 주어진 시간에 산성 또는 알칼리성 일 수 있습니다.
그러나 일부 물질은 그들이있는 환경에 따라 산과 염기로 작용할 수 있습니다. 이것을 양서류 물질이라고합니다. 예를 들어, 물 (H2O)은 반응에 따라 산 또는 염기로서 작용할 수있다.
주목하는 것이 중요합니다 : 양서류 물질은 동시 산도 및 알칼리도 상태에 존재하지 않습니다. 그들은 단순히 상황에 따라 어느 쪽이든 행동 할 수있는 능력이 있습니다.