* 산소 (O) :산소에는 6 개의 원자가 전자가 있으며 옥셋을 완성하려면 2 개가 필요합니다. 물 분자 (HATE)에서 볼 수 있듯이 2 개의 공유 결합을 형성합니다.
* 탄소 (C) :탄소에는 4 개의 원자가 전자가 있으며 옥셋을 완성하려면 4 개가 더 필요합니다. 그러나, 2 개의 이중 채권 또는 1 개의 트리플 본드와 1 개의 단일 채권을 형성 할 수 있습니다. 이것은 이산화탄소 (CO₂) 및 아세틸렌 (C₂H₂)과 같은 분자에서 볼 수 있습니다.
* 황 (s) :황은 6 개의 원자가 전자를 가지며 종종 2 개의 공유 결합을 형성합니다. 이것은 황화수소 (HATS)에서 볼 수 있습니다.
* 질소 (N) :질소는 일반적으로 3 개의 공유 결합을 형성하지만 (암모니아에서와 같이, NHAT), 히드라진 (N₂H₄)과 같은 일부 경우에는 2 개의 공유 결합을 형성 할 수 있습니다.
주요 고려 사항 :
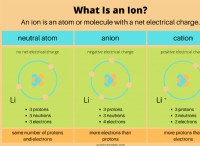
* 원자가 전자 : 원자가의 원자가 전자의 수는 얼마나 많은 결합을 형성 할 수 있는지 결정했습니다.
* 옥트 규칙 : 원자는 일반적으로 8 개의 원자가 전자를 갖기를 원합니다 (수소와 헬륨 제외, 2를 원하는).
* 전기 음성 : 관련된 원자의 전기성은 형성된 결합의 유형 (단일, 이중, 트리플)에 영향을 줄 수 있습니다.
원자 형태의 특정 결합 수는 일부의 분자에 따라 다를 수 있습니다.