이유는 다음과 같습니다.
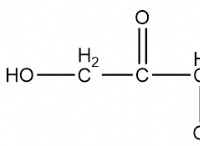
* 이온 성 화합물 : 칼슘 하이드로 겐 카보네이트는 이온 성 화합물이며, 이는 양으로 하전 된 칼슘 이온 (Ca²⁺)과 음으로 하전 된 수소 탄산염 이온 (HCO) 사이의 인력에 의해 형성됩니다.
* 극성 : 물은 극성 용매이므로 양의 및 부정적인 목적을 의미합니다. 이를 통해 이온 성 화합물과 상호 작용하고 용해시킬 수 있습니다.
* 용해도 규칙 : 일반적인 규칙은 그룹 1 (알칼리 금속) 또는 그룹 2 (알칼리 지구 금속) 양이온을 함유하는 대부분의 염이 물에 용해된다는 것입니다. 칼슘은 알칼리 지구 금속입니다.
그러나 캐치가 있습니다 :
* 평형 : 하이드로겐 카보네이트 칼슘의 용해도는 물에 이산화탄소 (CO2)의 존재에 의해 영향을받습니다.
* 이산화탄소 : CO2가 물에 용해 될 때, 그것은 탄산산 (H2CO3)을 형성하여 칼슘 하이드로겐 카보네이트와 반응하여 탄산 칼슘 (CACO3)을 형성하며, 이는 불용성 입니다. .
요약 :
* 칼슘 하이드로 겐 카보네이트 자체는 가용성이지만, 용해도는 CO2의 존재에 의해 영향을 받아 불용성 칼슘 탄산염이 형성됩니다. 그렇기 때문에 경수에는 종종 수소 카슘과 마그네슘 이온이 포함되어 있으며, 이온은 수소 카보네이트로 존재하지만 탄산염으로 침전 될 수 있습니다.