1. 유황 질화 :
* S4N4 (Tetrasulfur Tetranitride) : 이것은 밝은 노란색, 휘발성 및 폭발성 고체입니다. 그것은 질화 된 가장 흔한 황이며 다른 황 질소 화합물의 합성에 사용됩니다.
* s2n2 (Disulfur dinitride) : 이것은 쉽게 중합되는 매우 불안정하고 적신 고체입니다. 전기 전도성 중합체 인 폴리 (황 질화물)의 전구체이다.
2. 황 질소 헤테로 사이클 :
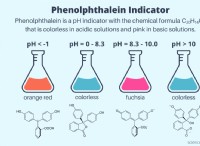
* 1,2,3,4- 시아트리아 졸 : 이것은 5 원 고리에서 황 원자와 3 개의 질소 원자를 함유하는 이종 세포 화합물입니다. 다양한 응용 프로그램이있는 무색의 고체입니다.
* 1,2,5- 티아 디아 졸 : 이것은 5 원 고리에서 황 원자와 2 개의 질소 원자를 갖는 또 다른 이종 세포 화합물입니다. 매운 냄새가 나는 무색 액체입니다.
3. 다른 화합물 :
* 질화염 (SO2N2) : 이것은 기체상에서만 알려진 불안정한 화합물입니다. 그것은 이산화황의 이산화 질소 반응에 의해 형성된다.
* 질소 황화물 (snx) : 이것은 황에서 질소 비율이 다양한 일련의 화합물을 의미합니다. 그것들은 일반적으로 반응성이 높고 불안정합니다.
황 질소 화합물의 특정 특성 및 적용은 크게 다릅니다. 일부는 반응성이 높고 폭발적이며 다른 일부는 비교적 안정적이며 흥미로운 전자 특성을 가지고 있습니다. 그들의 반응성과 불안정성은 다른 물질의 촉매, 폭발물 및 선구자로 유용하게 만듭니다.
황과 질소는 산소, 수소 및 탄소와 같은 다른 원소와 화합물을 형성 할 수 있음을 주목하는 것이 중요합니다. 이 화합물은 비료, 제약 및 산업 화학 물질을 포함하여 다양한 용도를 가질 수 있습니다.