이유는 다음과 같습니다.
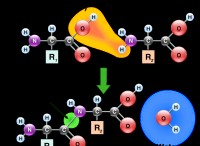
* 평형은 균형 상태입니다. 평형에서, 순방향 및 역 반응의 속도는 동일하다. 이는 반응물이 생성물로 전환되는 속도가 생성물이 다시 반응물로 전환되는 속도와 동일하다는 것을 의미합니다.
* 순 변경 사항이 없습니다. 속도는 동일하기 때문에 시간이 지남에 따라 반응물 또는 생성물의 농도에는 순 변화가 없습니다.
* 동적 프로세스. 농도가 정적으로 보일 수 있지만 반응은 여전히 일어나고 있습니다. 반응물은 지속적으로 제품으로 전환되고 있으며 그 반대는 마찬가지입니다.
예 :
간단한 반응을 고려하십시오.
a + b + c + d
평형에서, 반응물 (A 및 B) 및 생성물 (C 및 D)의 특정 비율이있을 것이다. 각각의 실제 양은 평형 상수 (k)에 따라 달라지며, 이는 평형에서 상대적인 생성물과 반응물을 알려줍니다.
키 포인트 : 평형은 반응이 중지된다는 것을 의미하지 않으며, 이는 전방 및 역 반응이 동일한 속도로 발생한다는 것을 의미하여 반응물 및 생성물의 양이 순 변화를 일으키지 않습니다.