electrophile :
* 정의 : electrophile은 전자 결핍 의 종입니다 따라서 는 전자가 풍부한 부위에 끌렸다 . 그들은 전자를 받아들이려고합니다 안정적인 전자 껍질을 달성하기 위해.
* 초점 : 초점은 전자 결핍 특성 에 있습니다 그리고 전자를 수용하는 능력 .
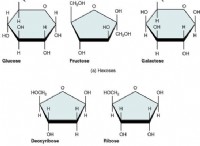
* 예 : 탄수화물, 양성자 (H+), 할로겐 (CL+, BR+등), 카르 보닐 화합물 (C =O) 및 알킬 할라이드.
루이스 산 :
* 정의 : 루이스 산은 가 전자 쌍을 받아들이는 종입니다 공유 결합을 형성합니다.
* 초점 : 초점은 전자 쌍을 받아들이는 능력 입니다. 결합 형성으로 이어집니다.
* 예 : 모든 전기성은 루이스 산이지만 모든 루이스 산이 전기성이 아는 것은 아닙니다. 예를 들어, ALCL3 및 FECL3과 같은 금속 양이온은 전자 쌍을 수용 할 수 있기 때문에 루이스 산이지만, 전기도와 같은 방식으로 전자가 풍부한 부위에 반드시 끌리는 것은 아닙니다.
주요 차이점 :
* 특이성 : 전기성은 루이스 산보다 더 구체적입니다. 그들은 특히 분자의 전자가 풍부한 부위에 끌립니다.
* 결합 형성 : 둘 다 전자를 받아들이는 반면, 전기는 새로운 결합을 형성하는 경향이있는 반면, 루이스 산은 복잡한 결합을 형성하거나 좌표를 형성 할 수 있습니다.
* 범위 : 모든 전기성은 루이스 산이지만 모든 루이스 산이 전기성이 아는 것은 아닙니다.
요약 :
* electrophiles는 Lewis Acids의 서브 세트입니다 . 그것들은 전자가 풍부한 부위를 선호하는 루이스 산입니다.
* 루이스 산은 더 넓은 범주입니다 . 그들은 복합체 형성 또는 좌표 결합을 포함하여 다양한 방식으로 전자 쌍을 받아 들일 수 있습니다.
이런 식으로 생각하십시오 :
* 모든 개는 동물이지만 모든 동물이 개가되는 것은 아닙니다.
* 모든 전기성은 루이스 산이지만 모든 루이스 산이 전기성이 아는 것은 아닙니다.