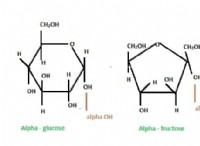
1. 이성질체를 이해하십시오
* 이성질체 동일한 분자 공식 (동일한 수와 원자 유형)을 갖지만 그 원자의 다른 배열을 갖는 분자입니다.
2. 부탄의 분자식
* 부탄은 분자 공식 c ₄h₁₀ 를 갖는다 .
3. 두 이성질체를 그립니다
* n- 부탄 (정상 부탄) :
* 다른 모든 원자가 부착 된 4 개의 탄소 원자의 직선 체인.
* 구조 :
```
H H H H
| | | |
C-C-C-C
| | | |
H H H H
```
* 이소 부탄 (2- 메틸 프로판) :
* 중심 탄소 원자가 3 개의 다른 탄소에 결합 된 가지 사슬.
* 구조 :
```
시간
|
H-C-H
|
H-C-C-H
|
시간
```
키 포인트 :
* 명명법 : "N- 부탄"의 "N"은 "정상"을 나타냅니다. "Isobutane"에서 "ISO"는 분지 구조를 나타냅니다.
* 번호 : 구조를 그리면 이성질체의 차이점을 볼 수 있도록 탄소를 숫자로하는 것이 도움이됩니다.
* 회전 : 단일 채권은 자유롭게 회전 할 수 있습니다. 따라서 다른 형태 (모양)로 n- 부탄을 그릴 수 있지만 모두 같은 분자로 간주됩니다.
다른 유기 화학 그림에 대한 도움을 원하시면 알려주세요!