1. 원자가 전자를 계산하십시오 :
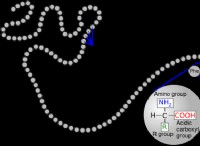
- 탄소에는 4 개의 원자가 전자가 있습니다.
- 질소에는 5 개의 원자가 전자가 있습니다.
- 수소는 각각 1 개의 원자가 전자 (총 3 개)를 가지고 있습니다.
- 총 :4 + 5 + 3 =12 원자가 전자
2. 중앙 원자를 결정하십시오 : 질소는이 분자에서 가장 전기 음성 요소이므로 중심 원자가 될 것입니다.
3. 원자를 단일 결합으로 연결하십시오.
- 질소를 3 개의 수소 원자에 연결하십시오.
- 질소를 탄소 원자에 연결하십시오.
4. 옥제를 완성하십시오 :
- 각 수소 원자에는 이제 2 개의 전자 (전체 듀엣)가 있습니다.
- 탄소 원자는 옥셋을 완성하기 위해 4 개의 더 많은 전자가 필요합니다.
- 질소 원자는 옥셋을 완성하기 위해 2 개의 더 많은 전자가 필요합니다.
5. 나머지 전자를 놓으십시오 :
- 질소 원자에 고독한 쌍을 놓습니다.
메틸 아민의 루이스 구조는 다음과 같습니다.
```
시간
|
H -C -N -H
|
시간
```
기억해야 할 중요한 점 :
* 탄소 원자는 4 개의 단일 결합을 형성합니다.
* 질소 원자는 3 개의 단일 결합을 형성하고 하나의 고독한 쌍을 가지고 있습니다.
* 각 수소 원자는 하나의 결합을 형성합니다.
이 구조는 수소 원자를 제외한 모든 원자에 대한 옥트 규칙을 충족시킨다.