화학적 결합에 의한 :
* 이온 성 화합물 : 반대로 하전 된 이온 사이의 정전기 인력에 의해 형성된다. 그들은 일반적으로 금속과 비금속을 포함합니다. 예 :NaCl (테이블 소금), mgcl2 (염화 마그네슘).
* 공유 화합물 : 원자 사이의 전자 공유에 의해 형성된다. 그들은 일반적으로 비금속을 포함합니다. 예 :H2O (물), CO2 (이산화탄소).
* 금속 화합물 : "전자 바다"에서 금속 원자 사이에 전자 공유에 의해 형성된다. 예 :금 (AU), 구리 (CU).
요소 수에 의해 :
* 이진 화합물 : 두 가지 다른 요소로 구성됩니다. 예 :H2O, NaCl.
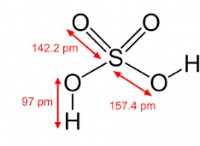
* 3 차 화합물 : 세 가지 다른 요소로 구성됩니다. 예 :H2SO4 (황산), NAHCO3 (중탄산 나트륨).
* 4 차 화합물 : 네 가지 요소로 구성됩니다. 예 :CH3COOH (아세트산).
기능 그룹에 의한 :
* 탄화수소 : 탄소와 수소 만 함유하는 화합물. 예 :메탄 (CH4), 에탄 (C2H6).
* 알코올 : 하이드 록실 (-OH) 그룹을 함유한다. 예 :에탄올 (C2H5OH), 메탄올 (CH3OH).
* Aldehydes : 탄소 사슬의 끝에 카르 보닐기 (-cho)를 함유한다. 예 :포름 알데히드 (HCHO), 아세트 알데히드 (CH3CHO).
* 케톤 : 탄소 사슬 내에 카르 보닐기 (-CO-)를 함유한다. 예 :아세톤 (CH3COCH3), 프로 파논 (CH3COCH2CH3).
* 카르 복실 산 : 카르 복실 그룹 (-COOH)을 함유합니다. 예 :아세트산 (CH3COOH), 포름산 (HCOOH).
* 아민 : 아미노기 (-NH2)를 포함합니다. 예 :메틸 아민 (CH3NH2), 에틸 아민 (CH3CH2NH2).
* 에테르 : 2 개의 탄소 사슬을 연결하는 에테르기 (-o-)를 포함합니다. 예 :디 에틸 에테르 (CH3CH2OCH2CH3), 디메틸 에테르 (CH3OCH3).
물리적 상태에 의한 :
* 고체 : 고정 된 모양과 볼륨이 있습니다. 예 :NaCl, Ice.
* 액체 : 고정 볼륨이 있지만 용기의 모양을 취하십시오. 예 :물, 수은.
* 가스 : 고정 된 모양이나 볼륨이 없습니다. 예 :산소, 질소.
다른 분류에 의한 :
* 유기 화합물 : 일반적으로 수소, 산소, 질소 및 기타 요소와 결합 된 탄소 원자를 함유합니다. 예 :포도당 (C6H12O6), 단백질, DNA.
* 무기 화합물 : 탄소 원자를 포함하지 마십시오 (탄산염 및 시안화물과 같은 몇 가지 예외 제외). 예 :NaCl, H2O, CO2.
이것은 단지 기본 개요 일 뿐이며 화합물의 더 자세한 분류가 많이 있습니다. 예를 들어, 유기 화학 내에서, 원자 및 기능 그룹의 특정 배열에 기초한 추가 분류가있다. 화합물을 분류하는 방식은 맥락과 이해가 가장 중요한 측면에 달려 있습니다.