공유 결합 이해
* 공유 전자 : 공유 결합은 둘 이상의 비금속 원자가 전자를 공유하여 안정적인 전자 구성 (보통 옥트)을 달성 할 때 형성됩니다.
* 비금속 : 공유 결합은 주로 비금속 (주기성 표의 오른쪽에있는 요소) 사이에 주로 발생합니다.
* 분자 화합물 : 공유 결합은 분자 화합물을 형성합니다.
공유 결합 공식을 작성하는 단계
1. 요소를 식별하십시오 : 화합물에 관련된 요소를 결정하십시오.
2. 원자가 전자 : 각 요소에 대한 원자가 전자 (가장 바깥 쪽 쉘의 전자)의 수를 알아야합니다. 이 정보는 주기율표에서 찾을 수 있습니다.
3. 옥트 규칙 : 대부분의 원자는 8 개의 원자가 전자를 갖기를 원합니다 (수소 제외, 2 개를 원하는).
4. 루이스 도트 구조 : 전자 공유 방식을 시각화하기 위해 Lewis Dot 구조를 그리십시오.
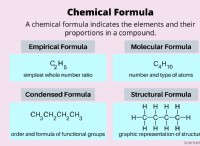
5. 경험적 공식 : 화합물에서 원자의 가장 간단한 전체 수비율을 나타내는 경험적 공식을 작성하십시오.
예 :물 (HATER)
1. 요소 : 수소 (H) 및 산소 (O)
2. 원자가 전자 : 수소는 1 개의 원자가 전자를 가지며 산소는 6 을가집니다.
3. 옥트 규칙 : 산소는 낙지를 완성하기 위해 2 개의 전자가 더 필요하며, 각 수소는 안정적인 구성을 달성하기 위해 하나의 전자가 하나 더 필요합니다.
4. 루이스 도트 구조 : 산소 원자가 중심에있는 구조를 그려 두 개의 수소 원자로 2 개의 공유 결합을 형성합니다.
5. 경험적 공식 : 가장 간단한 전체 수치 비율은 h₂o입니다.
키 포인트
* 접두사 : 공유 화합물의 이름을 지정할 때, 접두사 (mono-, di-, tri- 등)를 사용하여 각 유형의 원자 수를 나타냅니다. (예 :CO carbon은 탄소 *이산화탄소 *입니다).
* 예외 : 옥트 규칙에는 특히 8 개 이상의 원자가 전자를 가질 수있는 인 및 유황과 같은 원소가있는 예외가 있습니다.
* 다중 채권 : 일부 원자는 둘 이상의 전자를 공유하여 이중 또는 삼중 결합을 형성 할 수 있습니다.
더 많은 예제를보고 싶거나 공식을 작성하려는 특정 공유 화합물이 있으면 알려주세요!