* 이온 결합 하나의 원자 (일반적으로 금속)가 긍정적으로 하전 된 이온 (양이온)이되기 위해 전자를 잃고 다른 원자 (일반적으로 비 금속) 이득하여 전자가 음으로 하전 된 이온 (음이온)이 될 때 형태. 그런 다음 반대의 청구는 유인을 유치하여 채권을 형성합니다.
* 비금속 전기 음성이 높은 경향이있어 전자를 강력하게 끌어들이는 것을 의미합니다. 두 개의 비금속 결합이있을 때 전자를 완전히 옮기지 않고 공유합니다. 이 유형의 결합을 공유 결합 라고합니다 .
예 :
* 염화나트륨 (NaCl) : 나트륨 (금속)이 전자를 염소 (비금속)로 잃어 버리기 때문에 이것은 이온 성 화합물입니다.
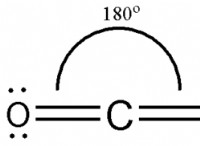
* 이산화탄소 (Co₂) : 탄소와 산소는 비금속이고 공유 전자이기 때문에 이것은 공유 화합물입니다.
예외 :
일반적으로 사실이지만 비금속이 이온 성 특성을 갖는 화합물, 특히 전기 음성의 상당한 차이를 형성 할 수있는 예외가 있습니다. 예제는 다음과 같습니다.
* 질소 트리오 오디 드 (NI₃) : 요오드는 비금속이지만, 질소와 요오드 사이의 전기 음성 성의 차이는 화합물이 일부 이온 성 거동을 나타낼 정도로 크다.
* 다 원자 이온 : 일부 다 원자 이온은 다수의 비 메탈을 함유하지만, 이온의 전체 전하는 이온 결합에서 단일 이온처럼 행동하게한다.
키 테이크 아웃 :
이온 성 화합물의 형성은 주로 금속과 비금속 사이의 전자의 전달에 의해 구동된다. 두 개의 비 메탈은 일반적으로 전자를 공유하여 공유 결합을 형성합니다.