전자 구성 :
* 1 ~ 3 개의 원자가 전자 : 금속 원자는 일반적으로 가장 바깥 쪽 에너지 수준 (원자가 전자)에 1, 2 또는 3 개의 전자를 갖는다.
* 상대적으로 낮은 이온화 에너지 : 그들은이 원자가 전자를 쉽게 잃어 양의 이온 (양이온)을 형성합니다. 이것은 전기와 열의 좋은 지휘자를 만듭니다.
물리적 특성 :
* 반짝임 : 금속은 빛과 상호 작용하는 방식으로 인해 광택이 있습니다.
* 가단성 : 그들은 깨지지 않고 얇은 시트로 망치질 수 있습니다.
* 연성 : 전선으로 끌어들일 수 있습니다.
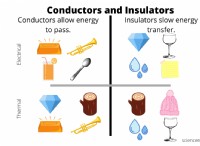
* 열과 전기의 좋은 지휘자 : 느슨하게 고정 된 원자가 전자는 열과 전기 에너지를 쉽게 전달할 수 있습니다.
* 실온에서 고체 (수은 제외) : 금속은 원자를 함께 고정하는 금속 결합이 강하기 때문에 강성 구조를 만듭니다.
* 높은 용융 및 끓는점 : 이러한 강력한 유대는 파손하기 위해 많은 에너지가 필요합니다.
화학적 특성 :
* 양이온 양식 : 금속은 전자를 쉽게 잃어 긍정적으로 하전 된 이온을 형성합니다.
* 비금속과 반응 : 금속은 비금속과 쉽게 반응하여 이온 성 화합물을 형성합니다.
* 형식 합금 : 금속은 함께 혼합되어 합금을 형성 할 수 있으며, 종종 특성이 향상됩니다.
작동중인 금속 특성의 예 :
* 금의 가단성 : 보석류 및 기타 응용 프로그램에 사용되는 엄청나게 얇은 시트로 망치질 수 있습니다.
* 구리의 전도도 : 전기 배선에 광범위하게 사용됩니다.
* 철의 강도 : 건설 및 인프라에 사용되는 강철의 핵심 요소입니다.
참고 : 이 속성에는 예외가 있습니다. 일부 금속은 가단성이 없거나 연성이 적고 일부는 융점이 낮습니다. 그러나 이는 대부분의 금속 요소를 설명하는 일반적인 특성입니다.