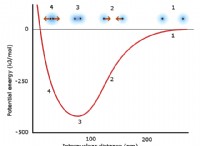
* 분자간 힘 : 아세톤 (CH3COCH3)은 강한 쌍극자 쌍극자 상호 작용을 갖는 극성 분자이며, 클로로포름 (CHCL3)은 극성이지만 염소 원자의 존재로 인해 런던 분산 력이 상당합니다. 이 두 액체가 혼합 될 때, 아세톤과 클로로포름 분자 사이의 강한 쌍극자-쌍극자 상호 작용은 각각의 순수한 액체 내의 개별 분자간 력보다 강하다. 이것은 혼합물에서 아세톤과 클로로포름 분자 사이의 더 강한 매력적인 힘을 유발하여 분자가 증기 상으로 빠져 나가기가 더 어려워집니다.
* 수소 결합 : 클로로포름은 수소 결합을 형성하지는 않지만 쌍극자 유발 쌍극자 상호 작용을 통해 아세톤의 산소 원자와 약하게 상호 작용할 수 있습니다. 이것은 혼합물의 분자간 인력을 더욱 향상시킵니다.
* Raoult의 법칙 : Raoult의 법칙은 용액의 증기압이 순수한 용매의 증기압을 곱한 용매의 두더지 분율과 동일하다고 명시하고있다. 그러나,이 법은 용질과 용매 사이의 분자간 힘이 각 순수한 성분 내의 것과 유사한 이상적인 솔루션에 적용됩니다. 아세톤 및 클로로포름의 경우, 혼합물의 더 강한 분자간 힘은 Raoult의 법칙에 의해 예측 된 것보다 더 낮은 증기압을 초래하여 부정적인 편차를 초래합니다.
요약 : 순수한 액체의 개별 분자간 힘과 비교하여 혼합물의 아세톤과 클로로포름 분자 사이의 더 강한 분자간 힘은 Raoult의 법칙에 의해 예측 된 것보다 더 낮은 증기압을 초래합니다. 이것은 액체 혼합물에서 이상적인 행동으로 인한 부정적인 편차의 전형적인 예입니다.