주요 차이 - 헬륨 대 수소
수소와 헬륨은주기적인 요소 테이블에서 발견되는 첫 두 요소입니다. 그러므로 그들은 지구상에서 가장 작고 가장 가벼운 원자입니다. 둘 다 기체 물질입니다. 수소와 헬륨의 특징적인 특징으로 인해 산업에서 이러한 가스의 많은 응용이 있습니다. 이 가스의 매우 가벼워서 공기 풍선을 채우는 데 사용됩니다. 헬륨과 수소의 주요 차이점은 헬륨 원자가 대기의 모노 토미 가스로 존재하는 반면, 수소는 대기에서의이 규정 가스로 존재한다는 것입니다.
주요 영역을 다루었습니다
1. 헬륨이란?
- 특성, 동위 원소, 반응 및 응용
2. 수소
- 특성, 동위 원소, 반응 및 응용
3. 헬륨과 수소의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 헬륨과 수소의 차이는 무엇입니까
- 주요 차이점 비교
주요 용어 :원자 질량, 원자 수, 중수소, 헬륨, 수소, 헬륨 동위 원소, 양성자, 삼중 수소 
헬륨
헬륨은 원자 번호 2가 있고 기체 물질 인 요소입니다. 헬륨의 화학적 상징은 그분입니다. 헬륨의 전자 구성은 1s입니다. 헬륨의 원자 상징은 2 입니다 그. 헬륨 원자는 핵에 2 개의 양성자와 2 개의 중성자와 1s 궤도의 2 개의 전자로 구성됩니다. 따라서, 헬륨의 원자 질량은 4.002602 AMU이다. 실온 및 압력에서 헬륨은 무색이며 무취 가스입니다. 헬륨은 우주에서 두 번째로 가장 풍부한 요소로 간주됩니다. 그것은 모노 토믹 가스로 존재합니다.
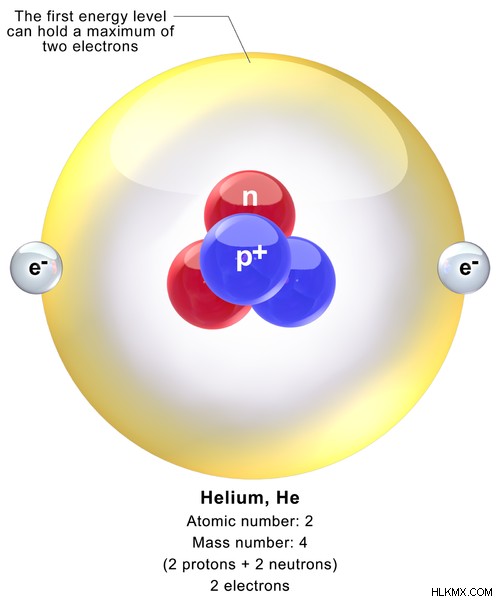
그림 1 :헬륨 원자의 화학 구조
헬륨의 융점은 약 -272.2c이며 이는 매우 낮습니다. 헬륨의 끓는점은 -268C로 제공됩니다. 이것은 더 넓은 범위의 온도를위한 가스입니다. 주기율의 요소 테이블에서 헬륨은 S 블록 요소로 분류되지만 테이블의 오른쪽 모서리에 배치됩니다. 헬륨은 화학 반응을 겪지 않는 불활성 가스이기 때문입니다. 또한 비금속입니다.
헬륨은 고귀한 가스이기 때문에 산화 상태가 0입니다. 헬륨의 알려진 두 가지 동위 원소가 있습니다. 그들은 동위 원소이고 동위 원소입니다. 그는 그들 중에서 가장 풍부한 형태이며 그 풍요는 99%로 주어집니다. 이들 동위 원소는 모두 안정적이며 방사성 붕괴는 관찰되지 않을 것이다. 그러나 다른 동위 원소도 있습니다. 그들은 불안정하고 방사성입니다.
헬륨은 풍선에 널리 사용됩니다. 또한, 헬륨은 높은 불활성으로 인해 많은 합성 반응 (예 :실리콘 결정의 합성)에 대한 제어 된 대기를 제공하는 데 사용됩니다. 또한 아크 용접을위한 불활성 방패로 사용됩니다. 헬륨은 액체 헬륨으로 알려져 있으며 중요한 극저온 물질로 사용되는 액체 형태로 전환 될 수 있습니다.
수소
수소는 원자 번호 1을 갖는 화학 요소이며 상징 H에 나와 있습니다. 수소 원자는 하나의 양성자로 구성되며 핵에는 중성자가 없습니다. 그것은 1s 궤도에 하나의 전자를 가지고 있습니다. 수소의 전자 구성은 1s로 주어진다. 수소는 주기율표의 S 블록 요소입니다. 수소의 원자 중량은 1.00794 AMU입니다.
실온과 압력에서 수소는 이원성 기체 분자로 존재합니다. 무색과 무취 가스입니다. 수소의 융점은 약 -259C입니다. 끓는점은 약 -252C입니다. 수소에는 3 개의 산화 상태가 있습니다. 그들은 -1, 0 및 +1입니다. 수소가 금속 원자에 부착되면 -1 산화 상태가 있습니다.
수소에는 세 가지 주요 동위 원소가 있습니다 :양성자, 중수소 및 삼중 수소. protium 가장 풍부한 동위 원소이며 풍부는 99%입니다. 그러므로 우리는 일반적으로 수소에 대해 이야기 할 때 양성자에 대해 이야기하고 있습니다. 중수소 또한 안정적인 동위 원소이지만 덜 풍부합니다. 그것은 핵에 중성자가 있고 양성자는 그렇지 않습니다. 삼중 수소 방사성 동위 원소입니다. 또한 안정적이지 않고 방사능이 높은 다른 동위 원소가 많이 있습니다.
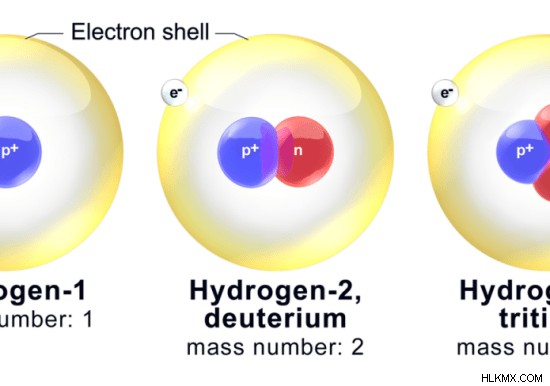
그림 2 :수소의 주요 동위 원소
수소 가스의 많은 응용이 있습니다. 화석 연료의 가공에 다량의 수소가 사용됩니다. 수소 가스는 또한 암모니아 생산에도 사용됩니다. 또한 수소는 발전소에서도 냉각수로 사용됩니다.
헬륨과 수소의 유사성
- 헬륨과 수소는 표준 온도 및 압력 조건에서 기체 물질입니다.
- 둘 다 1s 궤도 만 있습니다.
- 둘 다 작고 가벼운 물질입니다.
- 두 요소 모두주기 테이블의 S 블록에 속합니다.
- 둘 다 비금속입니다.
헬륨과 수소의 차이
정의
헬륨 : 헬륨은 원자 번호 2를 갖는 요소이며 기호로 표시됩니다.
수소 : 수소는 원자 번호 1을 갖는 화학 요소이며 기호 h.
로 표시됩니다.원자 번호
헬륨 : 헬륨의 원자 수는 2입니다.
수소 : 수소의 원자 수는 1입니다.
원자 중량
헬륨 : 헬륨의 원자 중량은 4.002602 amu입니다.
수소 : 수소의 원자 중량은 1.00794 AMU입니다.
화합물
헬륨 : 헬륨은 모나토미어 기체 물질로 존재합니다.
수소 : 수소는 규정 성 가스 분자로 존재합니다.
산화 상태
헬륨 : 헬륨은 산화 상태가 0 개뿐입니다.
수소 : 수소에는 -1, 0 및 +1 산화 상태가 있습니다.
동위 원소
헬륨 : 헬륨은 그와 He와 같은 두 가지 주요 동위 원소를 가지고 있습니다.
수소 : 수소에는 3 개의 주요 동위 원소가 있습니다. 양성자, 중수소 및 삼중 수소.
용융점
헬륨 : 헬륨의 융점은 -272.2c입니다.
수소 : 수소의 융점은 -259C입니다.
결론
헬륨과 수소는 매우 낮은 용융 및 끓는 온도로 인해 대기에서 기체 물질로 주로 발견되는 화학 요소입니다. 헬륨과 수소의 주요 차이점은 헬륨 원자가 대기의 모노 토미 가스로 존재하는 반면, 수소는 대기의 규정형 가스로 존재한다는 것입니다.