분자
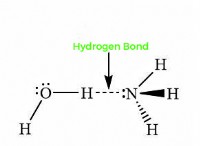
* 형성 : 둘 이상의 비금속 원자 사이의 전자 공유에 의해 형성된다. 이 공유는 공유 결합을 만듭니다.
* 본딩 : 공유 결합은 원자들 사이의 전자 공유를 포함한다.
* 속성 :
* 일반적으로 용융 및 끓는점이 낮습니다.
* 종종 실온에서 가스 또는 액체.
* 전기 도체가 열악한 경향이 있습니다.
* 예 : 물 (HATE), 이산화탄소 (CO₂), 포도당 (CATER)
이온 성 화합물
* 형성 : 양으로 하전 된 이온 (양이온)과 음의 하전 된 이온 (음이온) 사이의 정전기 인력에 의해 형성된다. 이 명소를 이온 결합이라고합니다.
* 본딩 : 이온 결합은 한 원자에서 다른 원자에서 다른 원자로 전자를 전달하여 반대로 하전 된 이온을 생성합니다.
* 속성 :
* 일반적으로 높은 용융 및 끓는점.
* 일반적으로 실온에서 고체.
* 물에 용해되거나 녹을 때 전기를 전도하십시오.
* 예 : 테이블 소금 (NaCl), 염화 칼슘 (CaCl₂), 산화 칼륨 (k₂O)
다음은 주요 차이점을 요약 한 표입니다.
| 기능 | 분자 | 이온 화합물 |
| ---------------- | ------------------------------------------------------------------------------- |
| 형성 | 전자 공유 | 전자의 전달 |
| 본딩 | 공유 결합 | 이온 결합 |
| RT | 가스, 액체 또는 고체 | 일반적으로 단단한 |
| 녹는 점 | 더 낮은 | 더 높은 |
| 전도도 | 가난한 | 양호 (용해되거나 녹을 때) |
키 테이크 아웃 :
* 근본적인 차이는 원자가 함께 고정되는 방식에 있습니다.
* 분자는 공유에 의해 형성되는 반면, 이온 성 화합물은 전자를 전달함으로써 형성된다.
* 이러한 결합의 차이는 뚜렷한 물리적 및 화학적 특성으로 이어집니다.