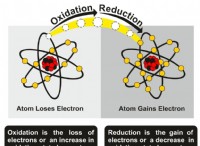
* 원자가 전자 : 이들은 원자의 가장 바깥 쪽 껍질에있는 전자입니다. 그것들은 화학적 결합에 관여하여 원자가 다른 원자와 어떻게 상호 작용하는지 결정합니다.
* 유사한 반응성 : 동일한 수의 원자가 전자를 갖는 요소는 유사한 유형의 화학적 결합을 형성하는 경향이 있으며 유사한 반응성을 갖는 경향이 있습니다. 예를 들어, 모든 알칼리 금속 (그룹 1)은 하나의 원자가 전자를 가지므로 반응성이 높고 전자가 양의 이온을 형성하기 쉽다.
* 유사한 결합 패턴 : 그것들은 유사한 원자가 전자 구성을 갖기 때문에, 동일한 그룹의 요소는 종종 유사한 구조 및 특성을 갖는 화합물을 형성한다. 예를 들어, 할로겐 (그룹 17)은 모두 7 개의 원자가 전자를 가지며, 음이온을 형성하기 위해 하나의 전자를 쉽게 얻어 유사한 이온 성 화합물을 초래한다.
예 :
그룹 1, 알칼리 금속을 고려해 봅시다.
* 리튬 (li) : 2, 1 (1 원자가 전자)
* 나트륨 (NA) : 2, 8, 1 (1 원자가 전자)
* 칼륨 (k) : 2, 8, 8, 1 (1 원자가 전자)
세 가지 요소 모두 하나의 원자가 전자를 가지므로 반응성이 높고 전자를 잃어 버리기 쉽습니다. 이것이 비슷한 화학적 특성을 공유하는 이유입니다.
요약 : 원자가 전자의 수는 요소의 화학적 거동을 결정하는 기본 요인입니다. 주기성 테이블의 동일한 패밀리의 요소는 동일한 수의 원자가 전자를 가지므로 유사한 화학적 특성, 결합 패턴 및 재 활성화를 초래합니다.