유기 화합물은 종종 흰색으로 보이므로 서로 구별 할 수 없습니다. 이것은 분자 내의 전자 전이 때문입니다.
어느 날, 당신은 모든 태블릿이 흰색 인 것처럼 보이기 때문에 당신이 잘못된 약을 먹었다는 것을 알고 있습니다. 당신은 당신에게 더 구별 가능한 약을주지 않은 것에 대해 의사를 비난합니다. 이것이 너무 많은 의약품이 이제 채색 된 이유입니다. 시각적으로 명백하고 를 구별 할 수 있도록 . 의약품은 주로 유기 화합물을 구성하며 대부분의 유기 화합물과 마찬가지로 무색/흰색입니다.
유기 화합물은 무엇입니까?
유기 화합물은 주로 탄소 (C) 및 수소 (H) 원자를 함유하는 분자입니다. 산소 (O), 질소 (N), 황 (S), 실리콘 (SI) 등과 같은 다른 원자는 또한 존재하지만, 첫 두 가지에 비해 낮은 양입니다.
이 원자는 유기 화합물을 고유 한 특성에 따라 다양한 그룹으로 특성화하는 데 도움이됩니다.
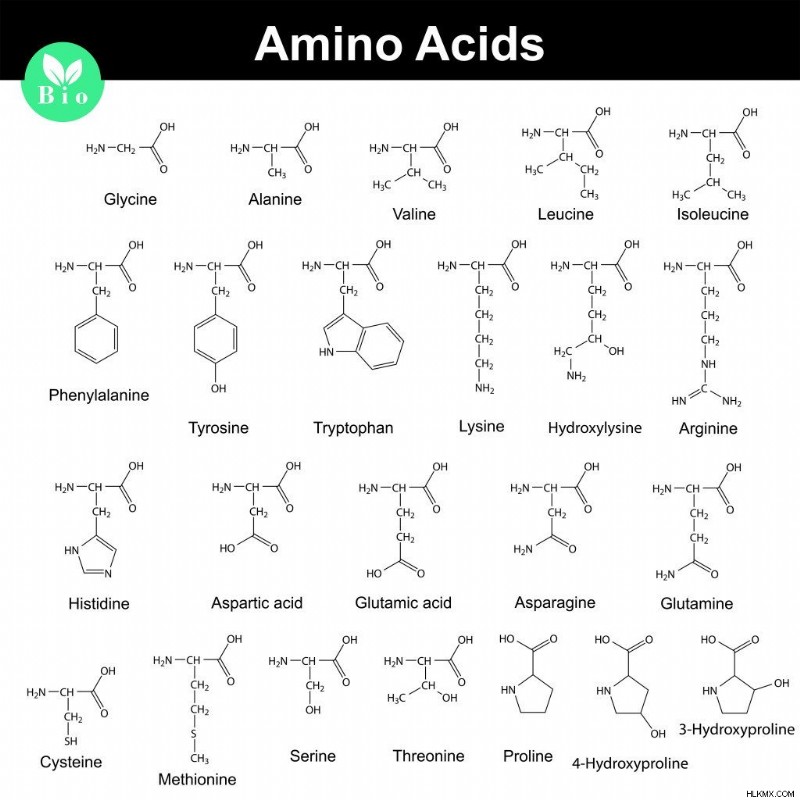
아미노산 목록 - 단순한 유기 화합물로 구성된 단백질의 빌딩 블록 (사진 신용 :염색체/셔터 스톡)
과거에는 생물이 풍부한 수의 유기 화합물로 구성되어 '유기농'이라는 용어를 얻었 기 때문에 과거에는 유기 화학이 '생명의 화학'인 것으로 생각되었습니다. '유기 화학'이라는 서사시 연구의 주인공은 Carbon, 입니다. 사 테라 벤시와 핵심의 주요 특성으로 인해.
오늘날 알려진 6 천만 개 이상의 유기 화합물이 있으며, 발견되거나 발명되기를 기다리는 더 많은 유기 화합물이 있습니다.
색상 이론
우리가 색상에 대해 이야기 할 때, 우리는 단순히“실제로 보이는 것이 존재하지 않는 것”을 기억하면됩니다.
터무니없는 소리?
하늘의 푸른 색과 티셔츠의 붉은 색을 분명히 볼 수 있습니다. 눈에 문제가 있다고 생각할 수도 있지만 그렇지 않습니다.
그러나 그것은 반대입니다. 당신이 보는 색은 실제로 입니다. 물질에 함유 된 색상은 대신 보완적인 색입니다. 이것은 반 직관적으로 들릴지 모르지만 사실입니다.
우리 주변에서 볼 수있는 색상은 모두 전자기 스펙트럼의 눈에 보이는 부분에 있습니다. 백색광 자체는 많은 색상의 스펙트럼이며 모든 색상/그늘은 해당 파장을 가지고 있습니다.
빛이 어떤 물질에 떨어지면, 그 중 일부는 흡수되고 나머지는 반사됩니다. 반사 된 빛은 우리의 눈에 도달합니다. 이것은 우리가 보는 색입니다.
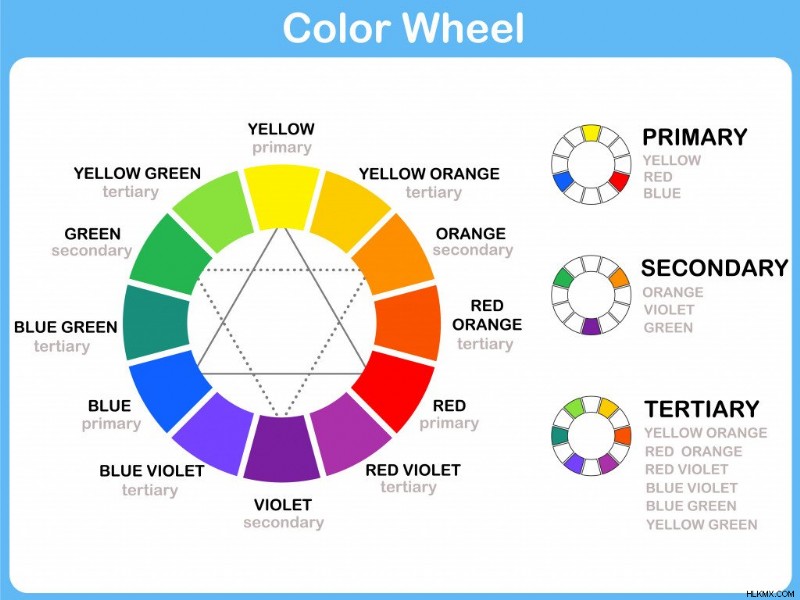
컬러 휠- 보완적인 색상을 나타내는 컬러 휠 (사진 크레디트 :Aekikuis/Shutterstock)
우리 중 많은 사람들이 미술 수업에서 본 컬러 휠이 이것을 보여줄 수 있습니다. 우리가 보는 색상, 흡수 된 보완 색상.
따라서 노란 꽃을 볼 때 실제로 흡수 된 색은 보라색입니다.
우리가 극단에 대해 이야기 할 때, 흰색으로 보이는 물질은 그것이 모든 파장을 반사했음을 나타내는 반면, 검은 색으로 보이는 물질은 모든 파장을 흡수하고 반사한다는 것을 의미합니다.
.UV-visible spectroscopy
분광법은 화학자들이 유기 분자의 구조와 그 특성을 이해하는 중요한 기술입니다. 이 기술에서, 원하는 분자는 전자기 방사선 (파장은 사용 된 분광법의 유형에 따라 다름)으로 조사된다.
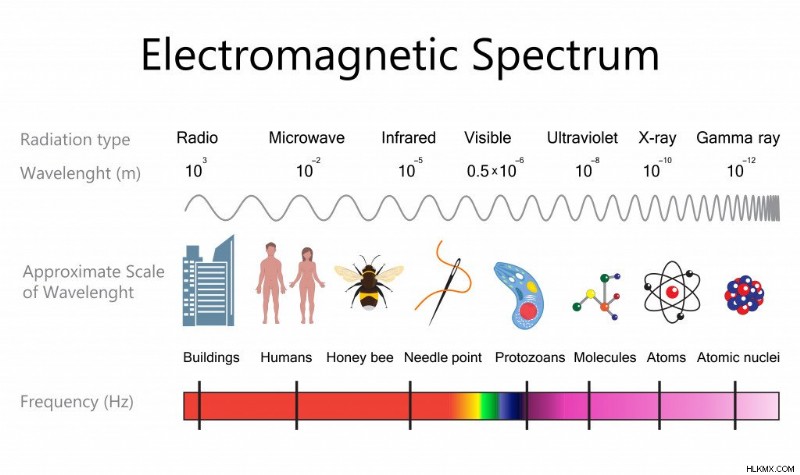
더 긴 파장 (왼쪽)에서 짧은 파장 (오른쪽)까지의 전자기 스펙트럼 (사진 크레디트 :멋진 tapis/shutterstock)
UV- 가시적 분광법은 주어진 화합물의 색상 특성을 연구하는 데 사용됩니다. 사용 된 파장은 200 nm - 800 nm 사이입니다. 200 nm 미만의 영역을 원수-ultraviolet 영역이라고하며 진공 조건이 필요하기 때문에 종종 연구가 적습니다. 화합물은 일련의 파장을 겪고 최대 흡수를 나타내는 파장은 λ 로 간주됩니다. Max. 가시적 영역에 있으면 상보적인 파장이 보입니다.
전자 전환
UV 분광법에서 전자 전이가 가장 중요합니다. 결합 된 전자는 입사 파장에서 에너지를 얻고 충분하면 더 높은 에너지 수준으로 홍보됩니다. 그림에서 볼 수 있듯이 관련된 본드 유형에 따라 전자는 여러 층으로 흥분됩니다.
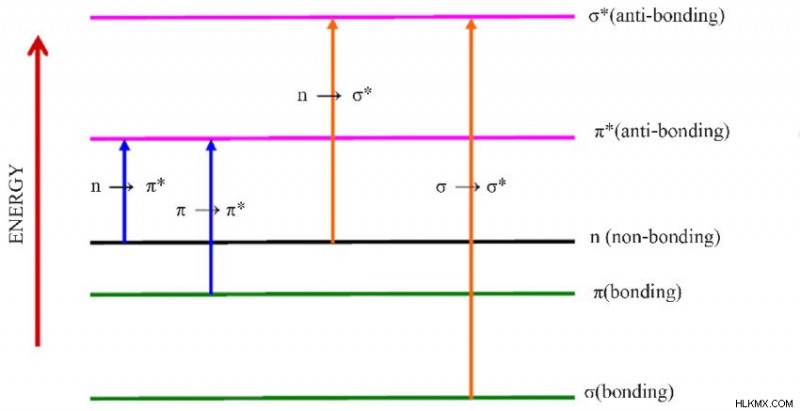
입사 파장으로부터의 에너지 흡수로 인한 전자 전이. (사진 크레디트 :크리에이티브 커먼즈)
| 전환 | 의미 |
| σ → σ* | 시그마 본드 전자 시그마 반 결합 궤도로 촉진 된 시그마 본드 전자 |
| n → σ* | 비 결합 전자는 시그마 안티 결합 궤도로 촉진 |
| π → π* | π 전자는 항 결합 π orbital | 로 촉진되었습니다
| n → π* | 비 결합 전자는 항 결합 π orbital | 로 촉진됩니다