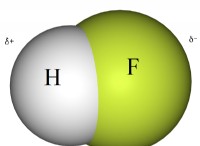
* 수소 결합 : 물 분자는 극성이며, 이는 약간 양의 말단 (수소 원자)과 약간 음의 말단 (산소 원자)을 의미합니다. 이러한 반대 전하는 물 분자 사이의 수소 결합을 형성하여 유치합니다.
* 강력한 명소 : 수소 결합은 상대적으로 강한 분자간 힘입니다. 이 강력한 관광 명소는 극복해야 할 상당한 양의 에너지가 필요하므로 물의 끓는점이 높습니다 (100 ° C 또는 212 ° F).
* 비교 : 수소 결합이 없으면 물은 메탄과 같은 다른 소분자 (끓는점 -161.5 ° C 또는 -258.7 ° F)와 비슷한 온도에서 끓입니다.
요약 : 물 분자들 사이의 강한 수소 결합은 파손하기 위해 많은 에너지를 필요로하며, 이는 왜 물이 다른 물질에 비해 상대적으로 높은 비등점을 갖는지를 설명합니다.