1. 열과 전기의 가난한 도체 : 비금속은 일반적으로 열과 전기의 열악한 도체입니다. 전자가 원자에 단단히 결합되어 자유롭게 흐르지 않기 때문입니다.
2. 고체 상태에서 취성 : 비금속은 종종 부서지기 쉬우므로 스트레스를받을 때 쉽게 파손됩니다.
3. 둔한 외관 : 대부분의 비금속에는 반짝이는 금속 광택이 없습니다. 그들은 종종 둔 해 보이거나 반사 표면이 있습니다.
4. 실온에서 가스 또는 액체 : 많은 비금속은 실온에서 가스로 존재하며 (산소 및 질소와 같은) 일부는 액체 (브롬)입니다. 비금속이 적은 비금속은 실온에서 고체입니다.
5. 저밀도 : 비금속은 일반적으로 금속보다 밀도가 낮습니다.
6. 화학 반응에서 전자를 얻는 경향이있다 : 비금속은 종종 화학 반응에서 전자를 얻음으로써 음성 이온 (음이온)을 형성하므로 전기 음성으로 간주됩니다.
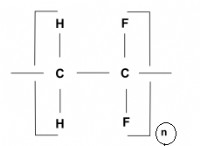
7. 산성 산화물을 형성 : 비금속이 산소와 반응하면 산성 산화물을 형성합니다. 예를 들어, 이산화황 (SO2)은 황산을 형성하기 위해 물에 용해되는 가스입니다 (H2SO3).