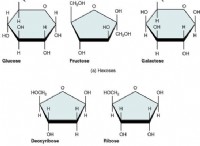
구조 및 결합 :
* 순환 : 그것들은 링에 6 개의 탄소 원자를 갖는 폐쇄 링 구조를 가지고 있습니다.
* 평면 : 고리의 모든 원자는 같은 평면에 있습니다.
* 박대 된 전자 : 고리의 전자는 특정 탄소 원자 사이에 국한되지 않지만 전체 고리 전체에서 공유됩니다. 이 탈퇴는 링 구조 내의 원으로 표시됩니다.
* 공명 : 방향족 화합물은 공명을 나타내며, 이는 그들의 실제 구조가 여러 기여 구조의 하이브리드임을 의미합니다. 이 분산은 안정성에 기여합니다.
* 특정 PI 전자 수 : 그들은 hückel의 규칙을 따릅니다 , 이는 방향족 화합물이 총 (4n+2) Pi 전자를 가지며, 여기서 N은 정수이다 (예를 들어, 벤젠은 6 개의 pi 전자, n =1).
속성 :
* 높은 안정성 : 전자의 비편 재화는 다른 불포화 탄화수소와 비교하여 방향족 화합물을 비정상적으로 안정적으로 만듭니다. 이 안정성은 그들의 반응성이 낮습니다.
* 낮은 반응성 : 알켄 및 알킨과 비교할 때, 이들은 비편성 전자 시스템으로 인해 첨가 반응에 대해 덜 반응성이있다.
* 전자 성 방향족 치환 : 방향족 화합물은 전기성 방향족 치환 반응을 겪고, 전기성 (전자 추구 종)은 고리의 수소 원자를 대체합니다.
* 특성 스펙트럼 특성 : 방향족 화합물은 분비 된 전자 시스템으로 인해 특징적인 UV-Vis 및 NMR 스펙트럼을 갖는다.
예 :
* 벤젠 (C6H6) : 가장 간단한 방향족 탄화수소와 클래스의 원형.
* 톨루엔 (C7H8) : 메틸기 부착 된 벤젠.
* 나프탈렌 (C10H8) : 두 개의 융합 벤젠 고리.
* 안트라센 (C14H10) : 3 개의 융합 벤젠 고리.
* 페놀 (C6H5OH) : 하이드 록실 그룹을 갖는 벤젠.
응용 프로그램 :
* 연료 : 많은 방향족 탄화수소는 휘발유 및 디젤과 같은 연료로 사용됩니다.
* 화학 물질 : 방향족 화합물은 플라스틱, 수지, 염료, 제약 및 폭발물을 포함한 다양한 화학 물질을 제조하는 데 사용됩니다.
* 용매 : 방향족 화합물은 많은 산업 공정의 용매로 사용됩니다.
참고 : 많은 방향족 화합물은 쾌적한 냄새가 있지만 "방향족"이라는 용어는 실제로 화학 구조를 지칭하며 반드시 향기와 관련이있는 것은 아닙니다.