바나듐은 주기성 테이블의 원자 번호 23이며 요소 기호 V가 있습니다. 역사적으로 자동차 몸체에 강한 강철을 만드는 데 사용되는 반짝이는 단단한 전환 금속입니다. 이 바나듐 사실에는 일반 정보 및 역사와 함께 화학 및 물리적 데이터가 포함됩니다.

기본 바나듐 사실
이름 : 바나듐
원자 번호 : 23
요소 기호 : v
그룹 : 5
기간 : 4
블록 : d
요소 가족 : 전이 금속
원자 질량 : 50.9415 (1)
전자 구성 : [ar] 3d4sfull :1S2S2P3S3P3D4S (Full)
발견 : 1801 년 Andres Manuel Del Rio
Del Rio는 멕시코 시티의 Royal School of Mines의 광물학 교수로서 광석을 포함하는 리드에서 새로운 요소라고 생각하는 것을 발견했습니다. 그의 발견의 그의 원래 이름은 소금이 생산 한 다양한 색상 때문에 Panchromium이었다. 그는이 소금의 대부분이 가열에서 붉은 색으로 변하기 때문에 요소를 Erythronium (붉은 꽃의 라틴어)으로 바꿨습니다. Del Rio는 확인을 위해 그의 샘플을 파리로 배송했습니다.
1805 년 프랑스 화학자 Hippolyte-Victor Collet-Sescotils는 Del Rio의 리드 광석에 대한 그의 발견을 발표했습니다. 그는 델 리오의 요소가 새로운 요소가 아니라 불순한 크롬이라고 말했다. 델 리오는이 분석을 받아들이고 그의 주장을 철회했다.
1830 년 스웨덴 화학자 Nils Gabriel Sefström은 그가 바나듐이라는 새로운 요소를 발견했습니다. 독일 화학자 Friedrich Wöhler는 Sefström의 바나듐이 Del Rio의 발견과 동일하다는 것을 보여주었습니다.
이름 원산지 : Vanadium은 스칸디나비아의 아름다움의 여신 인 Freyja의 노르웨이 이름 인 Vanadis의 이름을 따서 명명되었습니다.
동위 원소 :
천연 스칸듐은 하나의 안정적인 동위 원소 V와 하나의 거의 안정적인 동위 원소로 구성되어 있습니다. V. 24 인공 동위 원소가 발견되었습니다.
다섯
바나듐 -50은 25 개의 중성자를 함유하는 방사성 동위 원소입니다. Vanadium-50은 1.44 × 10 년의 반감기로 β 붕괴에 의해 β 붕괴에 의해 티타늄 -50으로 83%를 타이타늄 -50으로, 크롬 -50으로 17%를 감소시킨다. 천연 바나듐의 0.25%는 바나듐 -50입니다.
다섯
바나듐 -51은 바나듐의 유일한 안정적인 동위 원소이며 26 개의 중성자를 포함합니다. 천연 바나듐의 99.75%는 바나듐 -51입니다.

바나듐 물리 데이터
밀도 : 6.0 g/cm
용융점 : 2183 K (1910 ° C, 3470 ° F)
끓는점 : 3680 K (3407 ° C, 6165 ° F)
20ºC의 상태 : 단단한
융합의 열 : 21.5 kj/mol
기화의 열 : 444 kj/mol
어금니 열 용량 : 24.89 J/mol · K
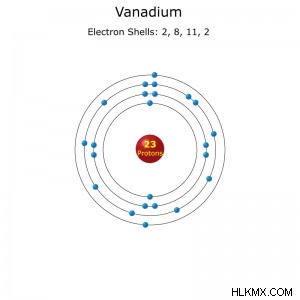
바나듐 원자 데이터
원자 반경 : 1.34 Å (경험적)
공유 반경 : 1.53 Å
van der waals 반경 : 2.07 Å
전자 친화력 : 50.655 kj/mol
전기 음성 : 1.63
1 이온화 에너지 : 650.908 kj/mol
2 이온화 에너지 : 1410.423 kj/mol
3 이온화 에너지 : 2828.082 kj/mol
4 이온화 에너지 : 4506.734 kj/mol
5 이온화 에너지 : 6298.727 kj/mol
6 이온화 에너지 : 12362.67 kj/mol
7 이온화 에너지 : 14530.7 kj/mol
8 이온화 에너지 : 16730.6 kj/mol
산화 상태 : +5, +4, +3, +2 (공통) +1, 0, -1 (드물지 않음)

재미있는 바나듐 사실
- 바나듐은 실온에서 중간 단단하고 연성, 반짝이며 강한 청색 회색 금속입니다.
- 바나듐은 원래 산화 상태의 이온에 의해 생성 된 다양한 색상 때문에 원래 Panchromium이라는 이름을 지었다. 사진은 +2, +3, +4 및 +5 산화 상태의 색상을 보여줍니다.
- 순수한 바나듐은 1869 년까지 영어 화학자가 될 때까지 생산되지 않았다.
- 대부분의 바나듐은 강을 강화하는 데 사용됩니다. 바나듐 스틸 합금은 엔진 부품, 갑옷 도금, 차축 및 도구에 사용됩니다.
- 바나듐은 자동차 산업에서 모델 T 포드를 구축하기 위해 광범위하게 사용되었습니다. 초기 모델 T 광고는 Vanadium Steel이 자동차 프레임 전체에서 제조되고 사용 된 가장 힘든 강철이라고 주장했습니다.
- 바나듐은 65 개의 다른 광물에서 발견됩니다.
- 바나듐은 낮은 중성자 흡수 특성으로 인해 원자로에 사용됩니다.
- 바나듐 펜 독 사이드 (V 2 o 5 ) 황산의 생산에서 촉매로 사용됩니다.
- 바나듐은 해양 생물의 혈액 세포에서 발견됩니다. 이 단백질은 바나빈으로 알려져 있습니다.
- 바나듐은 매우 소량의 필수 영양소이지만 바나듐 화합물은 대부분 인간에게 독성이있는 것으로 간주됩니다.
주기율표에서 요소에 대해 자세히 알아보십시오.