1. 낮은 반응성 :
* 파손하기 어려운 : H-H 결합의 높은 엔탈피는 그것을 깨기 위해 많은 에너지가 필요하다는 것을 의미합니다. 이것은 실온에서 수소 가스 (Hogen)가 상대적으로 반응하지 않습니다.
* 느린 반응 속도 : H-H 결합을 파괴하는 반응은 종종 필요한 높은 활성화 에너지로 인해 천천히 진행됩니다.
2. 특정 반응 경로 :
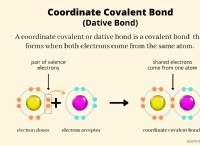
* 균질 분열 : H-H 결합이 파손되면 종종 동종이므로 각 수소 원자가 결합으로부터 하나의 전자를받습니다. 이것은 반응성이 높은 수소 라디칼의 형성으로 이어진다.
* 수소화 반응 : H-H 결합의 높은 엔탈피는 수소 가스를 좋은 환원제로 만듭니다. 전자를 다른 분자에 쉽게 기증하여 수소화 반응을 일으킬 수 있습니다.
3. 제한 반응 유형 :
* 고도로 전기 음성 원자와의 반응 : H-H 결합의 높은 엔탈피는 산소, 할로겐 및 질소와 같은 고도로 전기 음성 원자를 가진 사람들에 대한 반응을 제한합니다. 이들 원자는 H-H 결합으로부터 전자를 쉽게 끌어 당겨 새로운 화합물의 형성을 초래할 수있다.
* 유기 반응에 대한 제한된 참여 : H 그것은 반응성이 종종 너무 낮기 때문에 유기 반응에서 일반적으로 사용되지 않습니다.
4. 분자의 결합에 미치는 영향 :
* 분자의 더 강한 결합 : H-H 결합의 높은 엔탈피는 수 (HATE) 및 메탄 (CHAT)과 같은 수소를 포함하는 다른 결합의 강도에 기여한다.
5. 에너지 저장에 대한 시사점 :
* 잠재적 연료 공급원 : H-H 결합의 높은 에너지 함량은 수소를 유망한 연료 공급원, 특히 연료 전지와 같은 응용 분야에서 유망한 연료 공급원으로 만듭니다.
요약 :
H-H 결합의 높은 엔탈피는 수소 가스를 상대적으로 반응하지 않게하지만, 환원제로서 작용하고 수소화 반응에 참여하는 능력과 같은 특정 특성을 부여한다. 또한 수소와 관련된 다른 결합의 강도와 에너지 원으로서의 잠재력에 영향을 미칩니다.