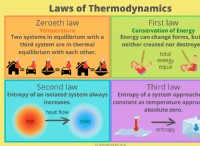
"가스의 온도와 양이 일정하게 유지되면 가스의 절대 압력과 부피는 반비례합니다.".
이런 일이 발생하는 이유는 다음과 같습니다.
* 더 많은 충돌 : 부피를 줄이면 가스 분자는 움직일 공간이 적습니다. 이는 용기 벽과 더 자주 충돌하는 것을 의미합니다.
* 힘 증가 : 각 충돌은 컨테이너 벽에 힘을 발휘합니다. 더 많은 충돌은 같은 지역에서 더 많은 힘이 가해지는 것을 의미합니다.
* 더 높은 압력 : 압력은 단위 면적당 힘으로 정의됩니다. 더 많은 충돌로 인해 힘이 증가함에 따라 압력도 증가합니다.
예 :
공기로 가득 찬 풍선을 상상해보십시오. 풍선을 짜면 볼륨을 줄입니다. 당신이 압박 할 때, 당신은 풍선이 압축하기가 점점 어려워지는 느낌이 들며, 이는 내부의 압력 증가 때문입니다.
수학적 관계 :
보일의 법칙은 수학적으로 다음과 같이 표현 될 수 있습니다.
p₁v₁ =p₂v₂
어디:
* p₁ =초기 압력
* v₁ =초기 볼륨
* p₂ =최종 압력
* v₂ =최종 볼륨
이 방정식은 부피 (v₂