유사성 :
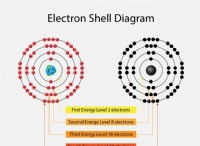
* 기간 3 : 세 가지 요소는 모두 주기율표의 세 번째 기간에 있습니다. 이것은 그들이 같은 수의 전자 쉘을 가지고 있음을 의미합니다 (3).
* 에너지 수준 수 : 각 원자에는 3 개의 주요 에너지 수준 또는 전자 쉘이 있습니다.
* 유사한 화학적 특성 : 한 기간 내에, 요소는 화학적 특성의 점진적인 변화를 보여줍니다.
차이점 :
* 그룹 번호 (원자가 전자) :
* 나트륨 (그룹 1A)은 1 개의 원자가 전자 (가장 바깥 쪽 쉘)를 갖습니다.
* 알루미늄 (그룹 3A)에는 3 개의 원자가 전자가 있습니다.
* 염소 (그룹 7A)에는 7 개의 원자가 전자가 있습니다.
* 금속 문자 :
* 나트륨은 반응성이 높은 금속입니다.
* 알루미늄은 또한 금속이지만 나트륨보다 덜 반응성입니다.
* 염소는 비금속, 반응성이 높은 가스입니다.
* 전기 음성 :
* 나트륨은 전기 음성 (전자를 유치하는 경향)이 낮습니다.
* 알루미늄은 중간 정도의 전기 음성을 가지고 있습니다.
* 염소는 전기 음성이 높습니다.
* 이온화 에너지 :
* 나트륨은 이온화 에너지가 낮습니다 (전자를 제거하는 데 필요한 에너지).
* 알루미늄은 중간 정도의 이온화 에너지를 가지고 있습니다.
* 염소는 이온화 에너지가 높습니다.
요약 :
나트륨, 알루미늄 및 염소는 모두 3 기간이지만 그룹 수는 화학적 특성에 상당한 변화를 가져옵니다. 나트륨은 반응성 금속이고, 알루미늄은 덜 반응성 금속이며, 염소는 반응성이 높은 비금속입니다. 이러한 차이는 주로 원자가 전자의 수와 전기 음성으로 인해 발생합니다.