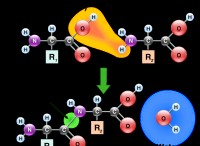
감소 에이전트 이해
* 감소 제 전자를 다른 물질에 기증하는 물질로, 전자가 줄어들게한다 (전자 게인).
* 전자를 기증하는 물질의 경향은 감소 전력 입니다. .
아연 대 수소
* 아연 (Zn) 수소 (H) 에 비해 전자를 잃는 경향이 더 높습니다. . 이것은 아연이 더 강한 환원제임을 의미합니다.
* 표준 감소 전위 (e °)에서 이것을 볼 수 있습니다.
* Zn² a (aq) + 2E⁻ → Zn (S) E ° =-0.76 V
* 2H⁺ (aq) + 2E⁻ → H₂ (g) E ° =0.00 V
변위 반응
* 더 높은 감소 전력은 아연이 용액에서 수소를 대체 할 수 있음을 의미합니다.
예를 들어, 아연 금속 조각을 산성 용액 (염산과 같은)에 넣으면 다음 반응이 발생합니다.
Zn (s) + 2H⁺ (aq) → Zn²⁺ (aq) + h₂ (g)
* 아연 (Zn)은 전자를 잃고 (산화되어 있음) Zn²⁺가됩니다.
* 수소 이온 (HAT)은 전자를 얻고 (감소 함) 수소 가스 (HAT)를 형성합니다.
키 포인트
* 표준 감소 전위가 부정적 일수록 감소 에이전트가 강해집니다.
* 강한 환원제는 화합물로부터 약한 감소 제를 대체 할 수 있습니다.
자세한 내용이나 예제를 원하시면 알려주세요!