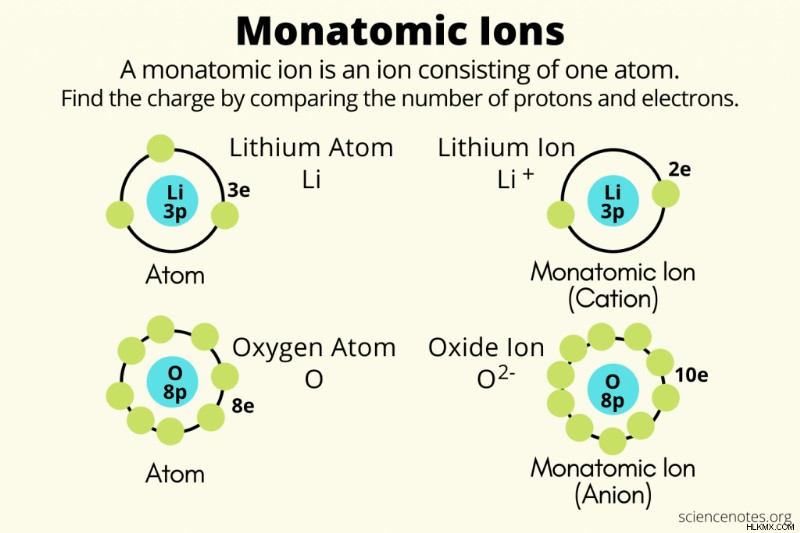
모나상 이온 정확히 하나의 원자로 만든 이온입니다. 다시 말해, 그것은 수의 양성자와 전자가 불평등 한 원자입니다. 전자보다 더 많은 양성자가있는 경우, 이온은 순 양전하를 가지며 양이온입니다. 양성자보다 더 많은 전자가있는 경우, 이온은 순 음전하가 있고 음이온입니다. 전형적으로 금속은 모나토미 양이온을 형성하는 반면 비금속은 모나토미닉 음이온을 형성합니다.
모나토미 이온 대 다항식 이온
이들 원자가 동일한 요소로 구성 되더라도 다 원자 이온은 둘 이상의 원자를 함유한다. 예를 들어, o 2 다 원자 이온 (보다 정확하게는 규조토 이온)입니다.
일부 사전은 "Monatomic"을 One Kind 을 언급하는 것으로 정의합니다. 하나의 원자가 아닌 원자의. 이것은 혼란을 초래할 수 있습니다!
모나토미 양이온 목록
다음은 공통 모나토미 양이온의 예입니다.
| 이름 | 기호 |
| 수소 | h |
| 리튬 | li |
| 나트륨 | na |
| 칼륨 | k |
| Rubidium | rb |
| cesium | cs |
| 마그네슘 | mg |
| 칼슘 | ca |
| strontium | sr |
| 바륨 | ba |
| 알루미늄 | al |
| 실버 | ag |
| 아연 | zn |
| 철 (II) | fe |
| 철 (III) | fe |
| 구리 (i) | cu |
| 구리 (II) | cu |
| 납 (II) | pb |
알칼리 금속은 +1 충전 및 알칼리 금속이 양이온을 형성하여 양이온이 +2 전하를 형성한다는 점에 유의하십시오. 대부분의 모나토미 이온은 금속이지만 금속성과 비금속의 모나상 이온도 있습니다.
모나토미네이션 목록
비금속은 대부분의 모나토미아 음이온을 형성합니다. 수소는 모나토미 양이온과 모나토미아 음이온을 모두 형성하는 요소의 예입니다. 다음은 일반적인 모나토미아 음이온 목록입니다.
| 이름 | 기호 |
| 수 소화물 | h |
| 불소 | f |
| 클로라이드 | cl |
| Bromide | br |
| iodide | i |
| 산화물 | o |
| 황화물 | s |
| 질화물 | n |
| 포스 파이트 | p |
모나토미 이온의 이름을 지정하는 방법
이름 지정 규칙은 모나토미 양이온 및 모나토미아 음이온에 대해 다릅니다.
Monatomic 양이온은 그들의 요소 이름에 따라갑니다. 이름에는 종종 요금이 포함됩니다. 이것은 원자가 둘 이상의 양이온을 형성 할 때 중요합니다. 예를 들어, 말하면 H는 "H plus 또는 h plus one"또는 "수소 플러스 또는 수소 플러스 1"이라고합니다. 칼슘 모나토미 이온 (CA)은 "CA + 2"또는 "칼슘 + 2"입니다. 둘 이상의 전하가 일반적이면 이름에는 원자의 산화 상태가 포함됩니다. 예를 들어, 모나상 구리 이온은 구리 (i) 또는 Cu (i) 및 구리 (II) 또는 Cu (II)입니다.
모나상 음이온에는 일반적으로 가변 전하가 없으므로 이름 지정이 더 간단합니다. 이름은 요소 이름의 첫 번째 부분이며 -ide 접미사가 이어집니다. 따라서 H는 수 소화물이고 N은 질화물 등입니다.
모나토미 이온이 형성되는 방법
원자는 화학 반응 동안, 이온 성 화합물이 녹을 때 및 전해질이 물에 해리 될 때 자연적으로 단일 분해 이온을 형성한다. 예를 들어, NaCl은 물에 용해 될 때 Monatomic 이온 Na 및 Cl-를 형성합니다. 원자는이 모나토미 이온을 형성하여 가장 안정적인 전자 구성을 갖습니다. 모나토미 이온은 반으로 채워 지거나 완전히 채워진 원자가 전자 쉘을 갖는 경향이 있습니다.
에너지를 첨가하면 모나상 이온이 형성됩니다. 그것은 분자의 원자 사이의 결합을 깨뜨 리거나 전자가 원자에서 벗어날 수있게한다 (이온화). 이 모나토미션 이온은 반응성이 높고 수명이 짧을 수 있습니다.
모나상 이온 vs 모나토미어 요소
예, 모나토미 이온이 요소의 이온입니다. 그러나 Monatomic Ion과 Monatomic 요소라는 용어는 다른 의미를 갖습니다.
모나토미어 요소는 전기적으로 중립적 인 단일 원자로 구성된 요소입니다. 모나토미어 요소의 친숙한 예는 고귀한 가스 원자입니다.
참조
- Cillispie, Charles (ed.) (1970). 과학 전기 사전 (첫 번째 ed.). 뉴욕시 :Charles Scribner의 아들. ISBN 978-0-684-10112-5.
- Knoll, Glenn F. (1999). 방사선 감지 및 측정 (3 판). 뉴욕 :와일리. ISBN 978-0-471-07338-3.
- 마스터 턴, 윌리엄; Hurley, Cecile (2008). 화학 :원리와 반응 . Cengage Learning. ISBN 0-495-12671-3.