이유는 다음과 같습니다.
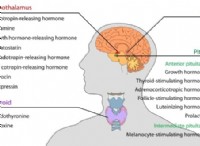
* 전자 구성 : 망간의 전자 구성은 [ar] 3d⁵ 4S²입니다. 3D 및 4S 궤도에서 7 개의 전자를 모두 잃어 버릴 수 있으며, 최대 산화 상태 +7 (MNI)을 초래할 수 있습니다. 예는 Mn이 +7 산화 상태를 갖는 칼륨 과망간산산염 (Kmno₄)을 포함한다.
* 철의 잠재력 : [ar] 3d⁶ 4S²의 구성을 갖는 철은 3D 및 4S 궤도에서 8 개의 전자를 모두 잃어 버릴 수있어 최대 산화 상태 +8 (Fe⁸⁺)을 초래할 수 있습니다. 그러나이 높은 산화 상태를 달성하는 것은 극히 드물며 산화 조건이 매우 필요합니다. 예를 들어 Fe가 +6 산화 상태를 갖는 화합물 칼륨 페레이트 (k₂feo₄)가있다.
* 다른 요인 : 높은 산화 상태의 안정성은 또한 원소의 전기 음성 성과 주변 리간드의 성질과 같은 인자에 의해 영향을받습니다.
요약 : 망간은 산화 상태가 매우 높지만 3D 시리즈에서 가장 높지는 않습니다. 철은 +8의 최대 산화 상태에 도달 할 수 있지만 덜 일반적입니다.