특성 :
* 에너지 입력 필요 : 반응은 주변 환경에서 에너지가 필요합니다. 이것은 열, 빛 또는 전기의 형태 일 수 있습니다.
* 냉각 효과 : 반응은 열을 흡수하기 때문에 주변의 온도가 감소합니다.
* 제품은 반응물보다 에너지가 더 높습니다 : 반응의 생성물은 반응물보다 더 높은 에너지 함량을 갖는다. 주변 환경에서 흡수되는 에너지는 제품의 화학적 결합에 저장되기 때문입니다.
예 :
* 얼음 용해 : 얼음은 주변에서 열을 흡수하여 액체 물로 녹입니다.
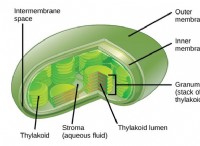
* 광합성 : 식물은 햇빛을 흡수하여 이산화탄소와 물을 포도당과 산소로 변환합니다.
* 질산 암모늄 용해 물에 : 용해 공정은 열을 흡수하여 용액을 차갑게 만듭니다.
흡열 반응에 영향을 미치는 요인 :
* 온도 : 온도를 늘리면 반응이 발생하기 위해 더 많은 에너지를 제공 할 수 있지만 반응 흡열을 유지하기가 더 어려워 질 수 있습니다.
* 압력 : 압력의 변화는 흡열 반응, 특히 액체 및 고형물과 관련된 반응에 미치는 영향을 최소화합니다.
* 촉매 : 촉매는 흡열 반응 속도를 높일 수 있지만 엔탈피 변화를 변화 시키지는 않습니다.
요약 :
양성 엔탈피 변화는 에너지 입력이 필요한 흡열 반응을 나타내고, 냉각 효과를 생성하며, 반응물보다 에너지가 높은 생성물을 나타냅니다. 이러한 특성을 이해하면 반응의 행동과 주변에 미치는 영향을 예측하는 데 도움이됩니다.