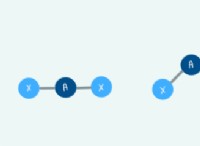
다음은 고장입니다.
CO2 :
* 중앙 원자 : 탄소 (C)
* 결합 원자 : 2 개의 산소 (O) 원자
* 중앙 원자에서 고독한 쌍 : 없음
* 모양 : 선형 . 결합 쌍을 반발하는 고독한 쌍이 없기 때문에, 2 개의 산소 원자는 가능한 한 멀리 떨어져있어 직선을 초래합니다.
H2O :
* 중앙 원자 : 산소 (O)
* 결합 원자 : 2 개의 수소 (H) 원자
* 중앙 원자에서 고독한 쌍 : 둘
* 모양 : 구부러진 또는 V 자형 . 산소 원자의 2 개의 고독 쌍은 수소를 가진 결합 쌍보다 더 강한 반발력을 가해 수소 원자를 함께 밀어 넣고 구부러진 모양을 만듭니다.
요약 :
형상의 차이는 중앙 원자에서 고독한 쌍의 존재로부터 발생한다. H2O에서. 이 고독한 쌍은 전자 구름 분포에 영향을 미치고 결합 각도에 영향을 미쳐 구부러진 모양을 만듭니다. CO2에서, 고독한 쌍의 부재는 원자의 선형 배열을 허용한다.
이 개념은 vsepr 이론 (Valence Shell Electron Pair 반발 이론)에 의해 설명됩니다. 이것은 중앙 원자 주위의 전자 쌍이 반발을 최소화하기 위해 자신을 배열 할 것이라고 명시하고 있습니다.