붉은 양배추 주스는 라임 주스를 뿌리거나 베이킹 소다 한 스푼을 넣을 때 색이 바뀝니다. 베이킹 파우더는 오븐에서 케이크가 아름답게 상승하게됩니다. 레몬과 라임 주스를 추가하여 물고기를 '요리'할 수 있습니다. 이것은 세비체를 만듭니다.
이 모든 예는 공통점이 무엇입니까?
그것들은 모두 산/염기 반응의 예입니다. 이러한 유형의 반응은 음식에서 발생하는 많은 화학 반응 중 하나 일뿐입니다 (다른 하나는 바나나의 갈색입니다). 산/기본 반응은 효과 (색상 변화, 누룩 케이크 또는 '요리 된'물고기)가 매우 다르게 보일지라도 공통점이 많습니다. 이 게시물에서는 이러한 반응 유형의 기본 과학에 대해 논의 할 것입니다.
식품 산성은 언제입니까?
산성 식품은 꽤 일반적입니다. 레몬 &라임 주스, 식초, 요구르트 및 버터 밀크는 모두 산성 음식입니다. 이 중 하나를 마시면 산도를 맛보세요.
산성 음식 (또는 음료)의 반대는 알칼리성입니다. 이것의 좋은 예는 베이킹 소다입니다. 산성이거나 알칼리성이 아닌 음식을 중성이라고합니다.
무언가가 산성인지 알칼리성인지 아닌지는 화학자에 의해 매우 잘 정의됩니다. 음식이 무엇인지 결정할 때 ph 스케일을 사용합니다. 이 척도는 0-14에서 실행됩니다. pH 값이 7 인 음식은 중립적입니다. pH가 7보다 낮은 음식은 산성이며, 7보다 높은 pH를 가진 음식은 알칼리성입니다.
그 중성 값 7에서 멀어 질수록 음식이 더 산성 (또는 알칼리성)입니다. 예를 들어, 레몬 주스의 pH 값은 2-3 인 반면 요거트의 주스는 약 4-4.5입니다. 따라서 레몬 주스는 요거트보다 더 산성입니다.
pH- 값 결정
pH- 미터 또는 특수 pH- 측정 스트립을 사용하여 식품의 pH 값을 측정 할 수 있습니다. ph-meter를 사용하는 경우 측정중인 제품에 대한 특정 값을 얻을 수 있습니다 (예 :2.3. 그러나 음식은 자연스럽게 매우 다양하기 때문에 비슷한 음식 사이에는 많은 변화가있을 수 있습니다. 하나의 레몬은 pH 값이 2.1 인 반면 다른 레몬은 2.4 일 수 있습니다. 그렇기 때문에 특정 음식에 대한 범위를 자주 보는 이유입니다.
식품의 pH- 값의 예
식품은 광범위한 pH 값을 가지고 있지만, 대부분은 7 (따라서 중립) 또는 7보다 낮지 만 대부분의 pH 값을 가지고 있습니다. 식품, 특히 과일 및 채소 및 고기와 같은 신선한 음식은 특성이 일정하지 않기 때문에 정확한 pH 값은 개별 품목마다 다릅니다. 많은 요인들이 pH 값에 영향을 미치며, 특히 농산물의 숙성에 영향을 미칩니다. 아래 목록은 몇 가지 일반적인 지침 (소스)을 제공합니다.
- 사과 :3,3 - 4,0
- 아보카도 :6,2 - 6,6
- 가지 :4,5 - 5,3
- 과일 잼 :3,5 - 4,5
- 꿀 :3,9
- 식초 :2,0 - 3,4
식품 과학에 사용되는 pH 값은 무엇입니까?
pH 값은 음식의 풍미에 영향을 미치지 만 음식의 유효 기간, 안전 유지 시간에도 매우 중요 할 수 있습니다. 바람직하지 않은 미생물의 성장으로 인해 음식은 망치고 나빠질 수 있습니다. 그러나 pH 값이 특정 값으로 침몰했을 때 많은 미세 유기체가 더 이상 자라지 않습니다. 따라서 pH 값을 충분히 낮추면 음식을 더 오래 유지할 수 있습니다.
저장 수명 외에도 pH 값은 식품 공정 모니터링에 사용될 수 있습니다. 예를 들어, 요거트를 만들면 주로 우유의 pH 값을 낮추는 것으로 구성됩니다. pH 값이 낮기 때문에 우유가 두껍게됩니다. 제조업체는 프로세스가 완료되는 PH 값을 알 수 있습니다. 이런 식 으로이 값을 측정함으로써 제품을 보거나 맛볼 필요없이 프로세스를 추적 할 수 있습니다.

pH 값
그렇다면이 음식을 알칼리성 또는 산성으로 만드는 것은 무엇입니까? 설탕은 달콤한 것을 만들고 소금은 짠맛을 만듭니다. 그것은 양성자가 산성을 만든 것입니다.
양성자
양성자는 전자를 놓친 단일 수소 원자 (H)입니다. 결과적으로, 그들은 긍정적으로 청구됩니다. 화학자들은 양성자를 다음과 같이 씁니다. h.
양성자는 인체와 그 문제에 대한 대부분의 살아있는 유기체에서 많은 반응에서 중요한 역할을합니다. 그래서 그들은 어디에서 왔습니까?
한 가지 방법은 자연적으로 산성 인 분자 (예를 들어, 구연산)를 통과하는 것입니다. 이것들은 그들의 양성자 중 하나를 매우 쉽게 벗어납니다. 그렇게하면 양성자의 농도가 증가합니다. 양성자의 농도가 증가하면 음식의 pH 값이 감소합니다. 더 많은 양성자는 더 많은 산도를 의미합니다. 이 관계는 다음 공식으로 표현할 수 있습니다.
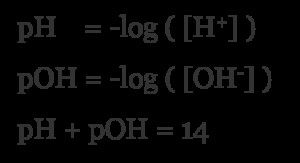
이 공식에서 볼 수 있듯이 양성자 (H)와 수산화 이온 (OH) 사이에는 균형이 있습니다. 그들은 서로의 반대입니다. 더 많은 양성자는 pH 값이 낮은 반면, 수산화 이온이 더 높은 pH 값 (또는 더 낮은 POH 값)을 초래한다. 가장 일반적으로 pH 값 만 찾을 수 있으며 POH 값은 실제로 거의 사용되지 않습니다. 이 관계는 산/염기 반응의 핵심이며 물 분자에서 기원합니다.
물과 산도
물 자체는 중립적이지만 양성자와 수산화물 이온 모두에서 분열 될 수 있습니다.

단수 양성자를 보는 대신, 히드로 늄 이온 (H 3 o) 형성됩니다. 물이있을 때 이것은 발생할 것이므로 많은 경우에 당신이 그것들을 교환 할 수있는 이유입니다. (화학 반응을 기록하는 데 익숙하지 않은 경우 화학 반응 기본 사항을 먼저 읽으십시오.)
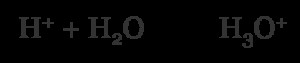
중성 환경에서는 동일한 양의 양성자 (H) 및 수산화 이온 (OH)이 있습니다. 음식이 산성 인 경우에만 알칼리성 이이 평형을 벗어납니다. 산성 분자 또는 알칼리성 분자는 양성자 또는 수산화물 함량을 증가시킬 수 있습니다.
산 (아래의 예에서 AH)이 물에 존재하면 양성자를 방출하여 pH 값을 감소시킵니다.

반면에 알칼리성 물질이 존재하면 수산화물 이온을 형성하여 수분이 더 많은 알칼리성이됩니다.

산/염기 반응
이 pH 값은 발생할 수있는 화학 반응의 유형에 대한 강력한 지표입니다. 알칼리성 환경이 아닌 산성 환경에서 다른 유형의 반응이 발생할 수 있습니다.
모든 산/염기 반응은 양성자가 교환된다는 공통점이 있습니다. 산은 양성자를 제공 할 것이다 (양성자의 농도를 증가시켜 pH를 낮추었다). 반면에 알칼리성 물질은 양성자를 복용하는 경향이 있습니다.
이전에 본 반응을 다시 살펴 보겠습니다. 이 양성자가 어떻게 교환되는지 살펴보십시오.


평형 반응
이 반응에서 알 수있는 한 가지는 둘 다의 이중 화살표입니다. 이 이중 화살표는 평형 반응임을 나타냅니다. 다시 말해, 반응은 왼쪽에서 오른쪽에서 오른쪽에서 왼쪽에서 왼쪽으로 발생할 수 있습니다. 이것이 양방향으로 같은 정도로 발생한다는 의미는 아닙니다.
매우 강한 산은 모든 양성자를 거의 (거의) 제공 할 것입니다. 이것들은 적절하게 강산이라는 이름입니다. 대부분의 경우 산의 일정 비율만이 양성자를 제공 할 것입니다. 이것들은 약산입니다. 알칼리성 상대 인베이스도 마찬가지입니다.
얼마나 많은 산이 양성자를 제공 할 것인지 평형 상수를 사용하여 발현 될 수 있습니다. 위에 표시된 산 (ah) 방정식의 경우 :
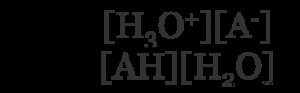
[]는 농도를 나타냅니다. 물의 농도는 사실상 일정하기 때문에 이것은 종종 방정식에서 제외됩니다. 거의 모든 양성자를 제공하는 산은 매우 낮은 농도의 Ah와 높은 농도를 가질 것입니다. 결과적으로, k a -값이 커질 것입니다. k a 가 클수록 -값, 산이 더 강해집니다.
이 평형 상수가 온도에 따라 변화한다는 것을 아는 것이 중요합니다. 따라서 산은 다른 온도에서 양성자를 쉽게 또는 덜 방출 할 수 있습니다.
알칼리성 물질의 경우 평형 방정식이 매우 유사합니다.

산/염기 반응 적용
실제로 당신은 k a 에 대해 논의하지 않습니다 및 k b 자주 가치. 그러나, 당신은 당신 주위의 모든 영향을 볼 것입니다. 예를 들어 베이킹 소다는 알칼리성 식품 성분의 예입니다. 이러한 기본 공식과 이러한 화학 반응을 비교하면 많은 유사성이 나타납니다.
붉은 양배추도 마찬가지입니다. 붉은 양배추의 색은 주변 액체의 pH 값으로 변합니다. 이것은 붉은 양배추에 색을 입히는 분자와의 산/염기 반응으로 인해 발생합니다!
물론 산은 화학 반응에 관한 것이 아닙니다. 또한 접시의 풍미와 균형에 관한 것입니다. 일부 요리는 잘 작동하기 위해 산 (예 :레몬 주스) 만 있으면됩니다. Samin Nosrat는 그녀의 책 Salt, Fat, Acid, Heat.
참조
Clemson University, 일반적인 식품 및 성분의 pH 값, 링크; 이 기사에서 언급 된 식품의 pH 값 소스