전해질의 몇 가지 예는 다음과 같습니다.
* 소금 : 테이블 염 (NaCl), 염화 칼륨 (KCl) 및 황산 마그네슘 (MGSO4)이 일반적인 예입니다.
* 산 : 염산 (HCl), 황산 (H2SO4) 및 질산 (HNO3)은 물에 완전히 분리되는 강산제입니다.
* 베이스 : 수산화 나트륨 (NaOH), 수산화 칼륨 (KOH) 및 수산화 칼슘 (CA (OH) 2)는 물에 완전히 분리되는 강한 염기입니다.
작동 방식 :
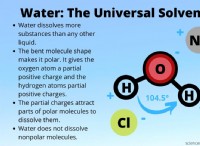
전해질이 물에 용해 될 때, 분자는 양으로 하전 된 이온 (양이온) 및 음이온 (음이온)으로 분리됩니다. 이 이온은 용액 내에서 자유롭게 움직일 수 있으므로 전기가 흐를 수 있습니다.
전해질이 아닌 것 :
가 아닌 물질 물과 혼합 될 때 전기 전기는 비 전해질 라고 불립니다 . 이 물질은 물에 용해 될 때 이온으로 분리되지 않습니다. 예제는 다음과 같습니다.
* 설탕 : 자당 (테이블 설탕)은 물에 용해되지만 이온으로 분해되지는 않습니다.
* 에탄올 : 알코올은 물에 용해되지만 이온을 형성하지는 않습니다.
중요한 참고 : 용액의 전도도는 전해질의 농도에 의존한다. 더 높은 농도의 이온은 더 나은 전도도를 초래합니다.