바이러스는 빛을 여행합니다. 대부분은 유전자 물질과 숙주의 세포에 침입 할 수있는 몇 가지 도구 만 가지고 다니고 있습니다. 그 후에는 호스트 자체 기계를 납치하여 수천 개의 사본을 제조합니다. 최근 수십 년 동안 생물 학자들은이 습격이 어떻게 빠져 나온 지에 대한 명확한 그림을 얻었습니다. 많은 바이러스는 세포가 일상적인 작업을 제어하기 위해 보내는 메시지를 억제합니다. 이 정보 간섭은 공격 바이러스가 필요하지 않은 일부 셀룰러 기능을 종료하고 다른 셀룰러 기능을 강화합니다.
그러나 최근 샌디에고 캘리포니아 대학의 생물 학자들이 최근에보고 한 바이러스는 미묘하고 더 복잡한 일을합니다. 과학자들은 선천적 결함의 일반적인 원인 인 Cytomegalovirus에 감염된 세포를 보았습니다. CMV 감염은 세포 메시지를 차단하지 않습니다. 대신 팀은 콘텐츠를 변경했다고 팀은 밝혔다. 자연 구조 및 분자 생물학의 새로운 논문에서 , 그들은이 호스트 커뮤니케이션의 수천 가지 변경 사항을 자세히 설명합니다.
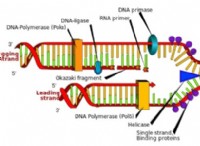
여기서 일어나는 일의 중요성을 이해하려면 먼저 세포가 정상적으로 작동하는 방식을 고려하십시오. 전체 사건의 핵심에는 DNA (세포의 모든 것을 만드는 방법에 대한 일종의 코드 북)이 핵의 자물쇠와 열쇠 아래로 유지됩니다. 세포가 단백질을 제조해야 할 때, DNA의 관련 부분이 전사됩니다. 메신저 RNA라고 불리는 그 전사 스크립트는 핵을 떠나 기계로 향하여 새로운 단백질을 만들기위한 템플릿으로 사용할 기계로 향합니다.
그러나 그 과정에서 RNA는 여러 가지 방법으로 편집 될 수 있습니다. 처리 방법에 대한 추가 지침을 제공하는 태그를 획득 할 수 있습니다. 부품이 튀어 나올 수 있습니다. 사용하기가 더 쉽거나 어려워지는 끝 부분을 얻거나 잃을 수 있습니다. 정상적인 방식으로, 셀은 이러한 모든 전략을 사용하여 자체 기능을 제어합니다. 실제로, 이들 RNA 메시지의 변경, 따라서 다른 버전의 단백질이 다른 시간에 이루어지는 것이 발달 과정의 핵심이다. 동일한 유전자는 인간 태아에서 단백질의 단백질과 성인의 다른 버전을 만드는 데 사용될 수 있습니다.
그러나 많은 것들과 마찬가지로, 일단 그 도구가 적의 통제하에 있으면 다른 이야기입니다. 호스트의 RNA 메시지를 편집 할 수있는 바이러스는 핵에 침입 할 필요없이 바이러스의 목표를 선호하는 단백질 버전을 만들 수 있습니다. 그리고 CMV는 다소 독특한 것으로 알려져 있기 때문에 - 분자 생물 학자 인 Gene Yeo와 바이러스 학자 인 Deborah Spector가 이끄는 UCSD 그룹은 호스트의 메시지를 억제하지 않는 바이러스 중 하나입니다.
먼저, 팀은 CMV로 인간 세포를 감염 시켰습니다. 그런 다음 감염 과정에서 다른 시점에서 세포에 의해 제조 된 RNA를 추출했습니다. 추출은 핵과 단백질 만들기 기계 사이의 수다의 합을 나타냈다. 그들은 건강한 대조군 셀과 비교하여 몇 개의 편집물 (추가 태그, 변경된 끝 조각 등)이 얼마나 많은지를 보았습니다. 감염의 초기 단계는 극적인 차이를 나타내지 않았지만, 감염된 세포가 버스트하고 새로운 바이러스의 톤을 방출 할 때 후반 단계는 다른 이야기였습니다.
.이 세포들은 제어에 나타나지 않은 2,500 개 이상의 변경을 보여 주었다.이 숫자는 논문의 첫 번째 저자이며 RNA 변화를 포함하는 질병을 연구 한 UCSD 연구원 인 Ron Batra를 놀라게했다. 바이러스가 그러한 변화를 일으킨다는 것은 놀라운 일이 아니지만, 결국 목표는 세포를 인수하는 것이며 바이러스 학자들은 한동안 이러한 변화의 개별 사례에 대해 알고있었습니다. 편집 횟수가 눈에 띄었습니다. 그는 일부 암이나 AL에서 볼 수있는 것처럼 정상에서 많은 변화가 있다고 말했다. 그는 100 개의 변화조차도“셀의 아키텍처를 많이 변화시키기에 충분하다”고 지적했다. "일부 질병에서는 세포를 죽이기에 충분합니다."
팀은 RNA를 변경하는 것으로 알려진 단백질을 식별하여 변화의 트리거를 검색했습니다. 연구자들은 특히 CPEB1이라고 불리는 하나가 감염된 세포에서 매우 높은 수준으로 존재한다는 것을 발견했습니다. CPEB1은 일반적으로 인간 세포에 의해 낮은 수준으로 만들어지며, 그 작업은 세포의 RNA를 조정하고 있습니다. 그러나 CMV가 도착하면 CPEB1의 숫자가 진행됩니다. RNA 연구의 선구자였던 Yale University의 생화학자인 Joan Steitz는 CPEB1 수준이 현저하다고 말했다. 그녀는 단백질 수준의 중간 정도의 변화가 중요한 것의 표식이라는 주장에 대해 일반적으로 회의적이라고 말하지만,이 연구는 감염된 세포가 CPEB1의 정상 양의 30 배를 가지고 있음을 보여줍니다. “이것은 거대한 입니다 그녀는 강조했다. “그래서 여기서 무슨 일이 일어나고 있습니다.”
이 과도한 CPEB1이 무엇을하고 있는지 확인하기 위해 팀은 건강한 세포에 일부를 추가했습니다. 이 세포들은 감염된 형제들에게서 볼 수있는 많은 변경을 계속했습니다. 그런 다음 연구원들은 감염된 세포를 가져 와서 CPEB1 수준을 인위적으로 줄였습니다. 세포의 바이러스의 수는 급락하고 세포는 또한 더 건강 해 보였다; 그들은 후기 감염의 부풀어 오르고 구근 모양이 없었습니다. 몇몇 관련 단백질을 사용한 유사한 실험은 동일한 효과를 생성하지 않았다. "바이러스는 CPEB1이없는 한 장애가 있습니다."구체적으로 "필요한 수준의 숙주 셀에서"
.그렇다면 바이러스 와이 단백질 사이의 연결은 정확히 무엇입니까? 여전히 불분명합니다. CPEB1은 RNA를 변형시키는 것으로 알려져있다. 그러나 CMV는 CPEB1을 사용하여 RNA를 편집하여 세포를 조작하여 바이러스에 직접 혜택을주는 특별한 버전의 숙주 단백질 (예 :단지 내버려 둘 수있는 면역 단백질 또는 크기의 단백질을 포장하는 것입니까? 또는 바이러스는 자체 유지 보수 과정의 일부로 단백질이 필요하기 때문에 CPEB1의 수준을 높이고 호스트에 대한 이러한 모든 변화는 부산물이기 때문입니까?
언뜻보기에 CMV 감염에 의해 변경된 많은 단백질에는 세포 포장이 포함되는 것으로 보이며, 이는 CPEB1이 바이러스의 이점을 위해 세포를 재생할 수 있다는 아이디어에 적합합니다. 그러나 실제로 그런지 알아 내기 위해 연구원들은 편집이 정확히 무엇인지, 그리고 호스트 셀이하는 일을 어떻게 변화시키는지를 자세히 살펴 봐야합니다.
.버클리 캘리포니아 대학교 (University of California)의 교수 인 브리트 글라운 싱거 (Britt Glaunsinger)는 바이러스와 관련된 바이러스를 연구한다고 말했다. Glaunsinger는“그들이 후속 조치를 취할 수 있거나 다른 사람들이 더 나은 사람이 기계적으로 후속 조치를 취하고 더 좋은 세부 사항을 얻을 수 있다면”라고 Glaunsinger는 말했습니다.
그러나 세포의 메시지와이를 조작하는 단백질을 살펴보면 유망한 전략이라고 바이러스가 그러한 단백질을 사용하는 방법을 연구 한 Steitz는 말했다. 그녀는“수천 개의 RNA- 결합 단백질이있다”고 말했다. "그들은 메신저 RNA의 삶에 정말 중요합니다." 그리고 그 RNA가 해석되는 방법은 건강한 세포와 병에 걸린 세포의 모든 차이를 만들 수 있습니다. 바이러스의 관점에서,이 메시지들은 세포를 통과하는 메시지, 쉽게 편집 할 수 있고, 교체 할 수있는 무수한 단백질은 그들의 끝을 달성하는 가장 큰 방법 일 것입니다. 실제로 UCSD 팀은 CMV와 관련된 Herpes Simplex Virus-2에 감염된 재 작업 된 호스트 세포 메시지를 발견했습니다. CPEB1은 이러한 경우에 관여하지 않았지만 많은 숙주 단백질이 이러한 변화를 만들기 위해 행동하도록 요청 될 수 있습니다.
Steitz는“이것은 바이러스가 들어가서 특정 단백질을 표적으로하는 또 다른 예일 뿐이며 자체 바이러스 성 RNA와 숙주 RNA에 중대한 영향을 미치며 전체 바이러스 황폐화 계획의 일부입니다. "매우 흥미로운 점은 다른 바이러스가 약간 다른 방식으로 수행한다는 것입니다."
.모든 RNA 결합 단백질이 잠재적으로 바이러스의 처분에 따라 적들은 우리의 세포의 메시지를 심오한 수정을하고있을 수 있지만 시간과 더 많은 작업 만 확실히 알 수 있습니다. Steitz는 그녀가 연구하고있는 헤르페스 바이러스에서 높은 수준의 CPEB1이 자라날 지 궁금합니다. 바이러스 성 인수의 끊임없이 변화하는 사례에서 따르는 또 다른 리드입니다.