화학에서 두더지 수량을위한 Si 기본 장치입니다. 이름에도 불구하고 작은 갈색/회색 정원 해충이나 멕시코 음식의 맛있는 초콜릿 소스와는 아무런 관련이 없습니다. 두더지 장치는 사물의 양 또는 수를 설명합니다.
두더지 정의 및 단위
2019 년 정의에 따라 두더지는 정확히 입니다 6.022 × 10.
1 몰 =6.022 x 10.
이 번호는 Avogadro의 번호입니다. 두더지에는 단위가 없습니다. 그것은 단지 무언가의 수를 설명합니다.
1 몰의 원자 =6.022 x 10 원자
1 몰의 물 =6.022 x 10 물 분자
1 몰의 두더지 =6.022 x 10 몰.
두더지의 목적
두더지의 목적은 매우 많은 수의 가치를 더 쉽게 만들고 있습니다. 결국, 6.022 x 10보다 1 몰을 쓰는 것이 훨씬 쉽습니다. 두더지 단위는 원자와 분자 사이를 전환하는 편리한 수단과 원자 또는 분자의 질량입니다. 두더지는 10 월 23 일 (10-23)에 두더지의 날을 축하하는 화학자들에게 충분히 중요합니다.
예제 두더지 계산
두더지를 사용한 화학 문제는 다음과 같습니다.
두더지 예제 문제 #1
단일 원자의 질량을 찾으십시오.
질문 : 질소의 단일 원자의 질량은 얼마입니까?
솔루션 : 원소의 원자 질량은 해당 요소의 한 두더지 그램의 질량입니다. 주기율표를 보면 질소의 원자 질량이 14.001 그램/두더지임을 알 수 있습니다.
이것은 1 몰의 질소 원자의 질량이 14.001 그램의 질량을 의미합니다.
1 몰의 N 원자 =6.022 x 10 N 원자 =14.001 그램.
방정식의 양쪽을 6.022 x 10 n 원자로 나누려면 하나의 질소 원자의 질량을 얻습니다.

1 n 원자 =2.325 x 10 g.
답변 : 하나의 질소 원자는 질량이 2.325 x 10 그램입니다.
두더지 예제 문제 #2
알려진 수의 분자의 질량을 찾으십시오.
질문 : 50 억 개의 물 분자의 그램에서 질량은 얼마입니까?
솔루션 :
1 단계 : 한 두더지의 물을 찾으십시오.
물은 h 2 입니다 따라서 O. 따라서 물의 질량을 찾으려면 수소의 질량과 산소 덩어리를 알아야합니다.
우리의 주기율표에서 우리는 1 몰의 수소 질량이 1.001 g이고 1 몰의 산소 질량은 16.00 g입니다.
1 몰의 물에는 2 몰의 수소와 1 몰의 산소가 있습니다.
1 몰의 물 질량 =2 (수소 질량) + 산소 1 질량
1 몰의 물 질량 =2 (1.001 g) + 16.00 g =18.002 g

2 단계 : 50 억 (5 x 10)의 물 분자를 찾으십시오.
이 부분에서는 Avogadro의 숫자를 비율로 사용합니다. 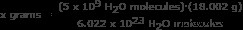
x 그램 =1.49 x 10 그램
답변 : 50 억의 물 분자는 질량이 1.49 x 10 그램입니다.
예제 문제 #3
주어진 질량에서 분자의 수를 찾으십시오.
질문 :15 그램의 얼음에 얼마나 많은 물 분자가 있습니까?
솔루션 :
1 단계 : 한 두더지의 물을 찾으십시오.
우리는 두 번째 예 에서이 단계를 수행했습니다. 물의 1 몰은 18.002 그램입니다.

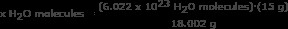
2 단계 : x h 2 에 대해 비율로 Avogadro의 숫자를 사용하십시오 o 분자
x h 2 o 분자 =5.018 x 10 h 2 o 분자
답변 : 15 그램의 얼음에는 5.018 x 10 물 분자가 있습니다.
참조
- 안드레아스, 버크; et al. (2011). "28SI 결정에서 원자를 세어 아 바가드로 상수의 결정". 물리적 검토 편지 . 106 (3) :30801. doi :10.1103/physrevlett.106.030801
- Bureau International des Poids et Mesures (2019). 국제 단위 (SI) (9th ed.).
- de bièvre, 폴; Peiser, H. Steffen (1992). “ '원자 무게' - 이름, 역사, 정의 및 단위”. 순수하고 응용 화학 . 64 (10) :1535–43. doi :10.1351/pac199264101535
- Himmelblau, David (1996). 화학 공학의 기본 원리 및 계산 (6 ed.). ISBN 978-0-13-305798-0.
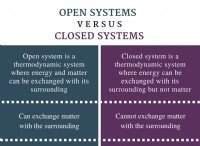
- yunus A. Çengel; Boles, Michael A. (2002). 열역학 :엔지니어링 접근법 (8th ed.). TN :맥그로 힐. ISBN 9780073398174.