과산화물의 이온 이온 이온의 방정식은 2Fe2+H2O2+2H+=2H2O+2Fe3+입니다. 과산화수소는 과산화수소와의 산화 환원 반응을 겪는다. 여기서 Fe²⁺는 환원제로서 작용하고 H₂O₂는 산화제로서 작용한다. 반응 동안, 환원제 Fe²⁺는 Fe³⁺로 산화되고, 산화제 h₂O₂는 H₂O로 감소된다.
과산화수소 소개
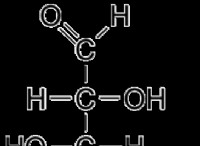
과산화수소의 화학적 공식은 H2O2입니다. 과산화수소는 어떤 비율로 물로 불만을 가질 수 있으며 강한 산화제입니다. 수용액을 과산화수소라고하며 투명합니다. 과산화수소는 종종 의료 소독 및 식품 소독 중에 사용될 수 있습니다.
과산화수소의 화학적 특성
1. 산화.
2. 환원성은 염소 및 칼륨 과망간산염과 같은 강한 산화제와 반응하여 산소를 형성한다.
3. 유기물이 발생한 후, 열로 인해 외국 공기와 물을 분해하고 크롬산, 칼륨 과망간산산염, 금속 및 탄산산과 격렬하게 반응합니다.
4. 순수한 과산화수소는 153 ° C로 가열되면 매우 불안정합니다.