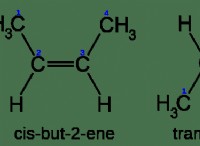
동종 트로프는 단일 화학 요소의 다른 구조적 형태로 정의됩니다. 이 형태는 원자가 서로 결합 할 수있는 다른 방법으로 인해 발생합니다.
스웨덴 화학자 Jöns Jakob Berzelius는 1841 년에 Allotropy의 개념을 제안했습니다.“Allotropy”라는 단어는 그리스어 단어 allotropia 에서 유래했습니다. , 이는“변화에 관한 것”을 의미합니다.
동종 요법은 무엇이며 어떻게 형성되는지
요소는 온도, 압력 및 빛에 대한 노출의 변화에 반응하여 한 할당에서 다른 동종으로 변형됩니다. 동반자는 종종 자발적으로 형성됩니다. 일반적으로, 용액 또는 용융물로부터 결정화되는 첫 번째 고체 동종은 가장 안정적인 것입니다. 이 현상은 Ostwald의 규칙 또는 Ostwald의 단계 규칙이라고합니다.
동종 트로프는 서로 다른 물리적 및 화학적 특성을 가지고 있습니다. 예를 들어, 다이아몬드와 흑연 (2 개의 탄소 동종)은 다른 외관, 경도 값, 녹는 점, 끓는점 및 재 활성을 갖는다.
일부 원소 동종 요소는 다른 분자 공식을 갖습니다. 형태 예, 이산 소 (o 2 ) 및 오존 (O 3 )는 고체, 액체 및 가스 단계에서 별도의 동화 로프로 존재합니다. 일부 요소는 고체상에서 다수의 동종 트로프를 가지고 있지만 하나의 액체 및 가스 형태를 갖는다. 다른 것들은 액체 및 가스 동화 로프를 가지고 있습니다.
동종 혈포의 예
대부분의 (아마도 모든) 요소에는 할당수가 있습니다. 동종이 가장 많은 요소는 여러 산화 상태를 가진 요소입니다. 비금속이 색상을 표시하는 경향이 있기 때문에 비금속의 동종상 동종이 가장 널리 인식됩니다. 그러나 메탈 로이드와 금속도 allotropes를 형성합니다.
다음은 다른 요소의 동화 로프의 예입니다. 연구자들은 항상 새로운 압력으로 형성된 새로운 동화 로프를 발견하고 있습니다.
탄소 동반 로프
- 다이아몬드 - 사면체 격자
- 흑연 - 육각형 격자 시트
- 그래 핀-2 차원 벌집 격자
- 비정질 탄소-비 결정자
- Lonsdaleite 또는 육각형 다이아몬드
- Fullerenes
- 나노 튜블
인 동종 호수
- 백색 인 - 결정질 테트라 파도 (p 4 )
- 붉은 인
- 바이올렛 인 - 모노 클리닉 결정
- 스칼렛 인
- 검은 인
- 디 포스포로스 - 기체 p 2
산소 동종
- dioxygen (o 2 ) - 무색 가스, 옅은 파란색 액체 및 고체
- 오존 (O 3 ) - 옅은 파란색 가스, 푸른 액체 및 고체
- Tetraoxygen (O 4 ) - 옅은 파란색에서 분홍색
- 옥타 독소 (O 8 ) - 붉은 결정
- Δ 상-오렌지
- ε- 위상-검은 색
- 금속성 - 매우 높은 압력으로 형성
비소 allotropes
- 노란색 비소-분자 비금속으로
4 - 회색 비소 - 중합체 AS (메탈 로이드)
- 흑인 비소-분자 및 비금속
TIN allotropes
- α-tin 또는 회색 주석-주석 해충이라고도합니다. 다이아몬드 입방 결정
- β- 틴 또는 흰색 주석
- γ-tin-신체 중심 정각 결정
- σ-SN-신체 중심 입방 결정
철분자
- α-fe 또는 페라이트-신체 중심 입방
- γ- 아이언 또는 오스테닌-얼굴 중심 입방
- δ- 아이언-신체 중심 입방
- ε- 아이언 또는 육각형-육각형 근접 포장
동종 vs 다형성
동종 영역은 다른 형태의 순수한 화학 요소를 말합니다. 다형성은 다른 분자 형태를 지칭한다. 포장 다형성은 분자가 다른 결정 구조를 나타낼 때입니다. 입체 형태 다형성은 이성질체화를 포함하여 동일한 분자의 상이한 준수제를 지칭한다.
다형성은 이진 금속 산화물, 예를 들어 Cro 2 에서 일반적입니다. , fe 2 o 3 및 al 2 o 3 . 다른 형태는 단계라고하며 일반적으로 그리스어를 구별하기위한 그리스어 문자가 있습니다. 예를 들어, cro 2 정사각형 α 상 및 사방 정하 β 상이 있습니다.
다형성은 의약품에서 일반적입니다. 종종 용해도와 치료 효과는 다형성에 대해 매우 다르므로 규제 승인은 단일 형태에 대한 경향이 있습니다.
O 2 에 대한 산소의 2 개의 동종 및 O 3 , 처음으로 인정받는 사람 중 하나였습니다. Ostwald는 할당량이 다형성의 특별한 경우로 간주했다. 그러나, 대부분의 화학자들은 다른 요소 형태를 동종 트로프로, 다른 분자는 다형성으로 지칭한다. 기술적으로, 분자 산소 (O 2 ) 및 오존 (O 3 )는 동반 로프와 다형성입니다.
참조
- iupac (1997). "동반자". 화학 용어의 개요 (제 2 판) (“골드 북”). doi :10.1351/goldbook.a00243
- Jensen, W. B. (2006). “이 용어는 동종의 기원”. j. 화학 교육 . 83 (6) :838–39. doi :10.1021/ed083p838
- Threlfall, T. (2003). "Ostwald의 규칙에 대한 구조적 및 열역학적 설명". 유기농 프로세스 연구 및 개발 . 7 (6) :1017–1027. doi :10.1021/op030026l