POH 및 PH는 수용액이 얼마나 산성 또는 기본인지를 설명하는 방법입니다. POH 정의는 다음과 같습니다. POH 및 PH가 어떻게 관련되어 있는지, POH 계산의 예
POH 정의
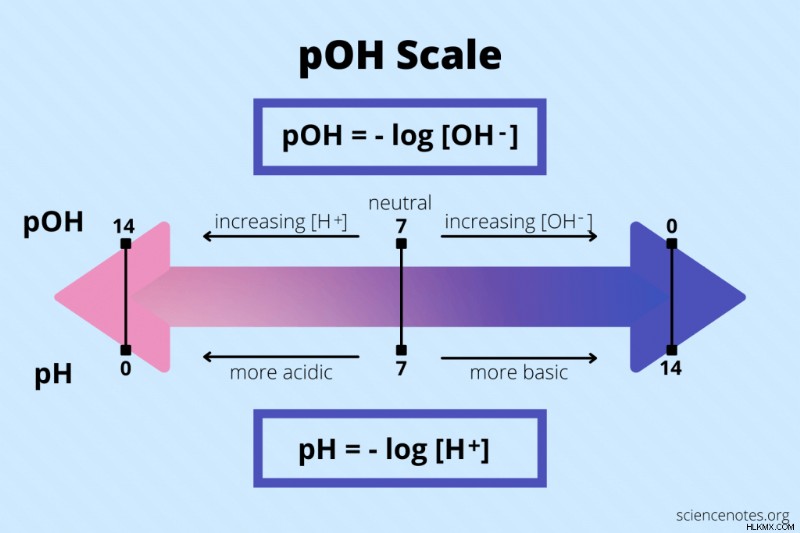
poh 수성 용액의 양은 수산화물 이온 (OH) 농도의 음성 로그입니다.
poh =-log [오]
pH와 마찬가지로, POH 값은 1에서 14이며, 여기서 7은 중성이다. pH와 POH의 척도는 서로 반대입니다. 낮은 POH 값은 알칼리도의 높은 염기성을 나타내고, 높은 POH 값은 높은 산도를 나타냅니다. 대조적으로, pH가 낮은 것은 높은 산도를 나타내고, 높은 pH는 높은 염기성을 나타냅니다.
왜 poh를 사용합니까?
pH는 이미 산과 염기를 묘사하는 편리한 방법이기 때문에 왜 POH를 사용하고 싶은지 궁금 할 것입니다. POH의 주요 사용은 용액의 pH가 알려져있을 때 수산화물 이온 농도를 찾고있다. 또한베이스의 POH를 계산 한 다음 pH를 계산하는 것이 더 쉽습니다.
pH와 POH가 어떻게 관련되어 있는지
PH와 POH는 관련이 있습니다. pH가 증가함에 따라 POH가 감소합니다. pH가 감소함에 따라 POH가 증가합니다.
- ph + poh =14 (25 ° C에서)
- pH =14 - POH
- poh =14 - ph
poh를 찾는 방법
POH를 찾는 두 가지 방법은 수산화물 이온 농도 또는 알려진 pH 값에서 나온 것입니다.
수산화물 이온 농도에서 POH를 찾으십시오
기본 솔루션의 몰토리성을 알고 있다면 POH 공식의 수산화물 이온 농도로 연결하십시오.
예를 들어, 0.25 M NAOH 솔루션의 POH를 찾으십시오.
여기서 핵심은 수산화 나트륨이 강한 염기임을 인식하는 것입니다. 따라서 농도는 수산화물 이온 농도입니다. 이것은 수산화 나트륨이 물의 이온에 완전히 분리되기 때문입니다 :
naoh ( aq ) → Na ( aq )+OH ( aq )
다시 말해, Naoh의 모든 두더지에 대해 용액에는 하나의 OH가 있습니다. 나오와 수산화 이온은 동일한 농도 값을 갖는다 :
[naoh] =[오]
따라서 POH 공식에서 수산화 나트륨 농도를 사용하십시오.
poh =-log [오]
poh =-log (0.25)
poh =0.60
대답과 그것이 의미가 있는지 생각해보십시오. 이것은 강력한 기본 솔루션이므로 pH 값이 높거나 POH 값이 낮습니다. 0.60의 POH는 매우 낮으므로 대답은 의미가 있습니다!
산의 농도가 주어지면 먼저 pH를 계산 한 다음 값을 사용하여 poh를 찾습니다.
pH
에서 poh를 찾으십시오예를 들어, pH 3.5 인 솔루션의 POH를 찾으십시오.
.
pH + poh =14
poh =14 - ph
poh =14 - 3.5
poh =10.5
참조
- Covington, A.K.; 베이츠, R. G.; Durst, R. A. (1985). "pH 척도, 표준 기준 값, pH 측정 및 관련 용어의 정의". 순수한 응용 프로그램. 화학 . 57 (3) :531–542. doi :10.1351/pac198557030531
- Feldman, Isaac (1956). "pH 측정의 사용 및 남용". 분석 화학 . 28 (12) :1859–1866. doi :10.1021/ac60120a014
- Mendham, J.; Denney, R. C.; 반즈, J. D.; Thomas, M. J. K. (2000). Vogel의 정량적 화학 분석 (6th ed.). 뉴욕 :프렌 티스 홀. ISBN 0-582-22628-7.