주요 차이 - 상대 원자 질량 대 원자 질량
원자는 물질의 기본 단위입니다. 과학적 발견은 원자가 전자, 양성자 및 중성자와 같은 아 원자 입자로 더 나눌 수 있음을 밝혀냈다. 또한 원자는이 핵을 주위로 움직이는 핵 및 전자라는 중심 코어를 갖는 복잡한 구조를 갖는 것으로 밝혀졌다. 핵에는 양성자와 중성자가 포함되어 있습니다. 상대 원자 질량과 원자 질량은 원자의 질량을 발현하는 데 사용되는 두 가지 화학 용어입니다. 상대 원자 질량과 원자 질량의 주요 차이점은 상대 원자 질량의 원소 원자의 평균 원자 질량의 평균 덩어리의 비율은 카본 -12의 질량의 12 분의 1의 비율 인 반면 원자 질량은 원자의 핵에 존재하는 핵의 총 질량이다. .
주요 영역을 다루었습니다
1. 상대 원자 질량
- 정의, 계산, 예
2. 원자 질량
- 정의, 계산, 예
3. 상대 원자 질량과 원자 질량의 차이는 무엇입니까
- 주요 차이점 비교
주요 용어 :원자, 원자 질량, 전자, 중성자, 핵, 양성자, 상대 원자 질량

상대 원자 질량
상대 원자 질량은 원소의 원자의 평균 질량의 비율과 카본 -12의 질량의 1 분의 1의 비율입니다. Carbon-12의 원자 질량의 12 분의 1은 원자 질량 단위 (1 amu 또는 1 u)로 명명됩니다. 따라서 Carbon-12의 상대 원자 질량은 12 amu입니다.
상대 원자 질량 =카본 -12 x의 원자/질량의 평균 질량 (1/12)
원자의 평균 질량은 요소의 다른 동위 원소의 질량과 풍부도를 사용하여 계산됩니다. Carbon-12 동위 원소의 질량 12 분의 1의 값은 1.66054 x 10g입니다. 그것은 1 u 또는 하나의 통합 원자 질량 단위와 같습니다. 수소 원자를 고려하고 상대 원자 질량을 계산해 봅시다.
수소의 상대 원자 질량
먼저, 우리는 수소 원자의 평균 질량을 찾아야합니다.
|
동위 원소
|
풍부 (%)
|
질량 (u)
|
|
수소 -1
|
99.98
|
1.007825
|
|
수소 -2
|
0.02
|
2.014101
|
|
수소 -3
|
추적
|
3.016049
|
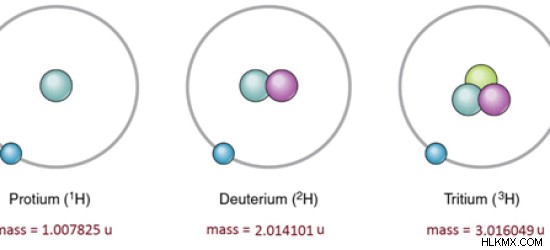
그림 1 :수소의 동위 원소
수소의 평균 질량 =(1.007825 U x 99.98 %) + (2.014101 U x0.02 %)
=(1.007623 + 0.00402) u
=1.0076632 u
Carbon-12 동위 원소 질량의 12 분의 1의 값은 1 u입니다.
따라서
상대 원자 질량 =카본 -12 X의 원자 /질량의 평균 질량 (1/12)
=1.0076632 u /1 u
=1.0076632
여기서, 삼상의 질량은 환경에서 풍부함이 미량이며 무시할 수 있기 때문에 계산에 포함되지 않았습니다. 최종 값은 상대 값이기 때문에 차원이 없습니다.
원자 질량
원자 질량은 원자의 핵에 존재하는 핵의 총 질량입니다. 핵은 양성자 또는 중성자입니다. 따라서, 원자 질량은 핵에 존재하는 양성자 및 중성자의 총 질량이다. 전자는 원자에도 존재하지만, 전자의 질량은 전자가 너무 작고 양성자 및 중성자와 비교할 때 무시할 수있는 질량을 가지기 때문에 계산에 사용되지 않습니다.
상대 원자 질량과 달리 평균 값을 계산하지 않고 각 원자의 질량을 계산합니다. 따라서, 우리는 다른 동위 원소의 원자 질량에 대해 다른 값을 얻습니다. 그것은 동일한 요소의 동위 원소에 존재하는 핵의 수가 서로 다르기 때문입니다.
상대 원자 질량과 동일한 예를 고려해 봅시다. 수소.
수소 -2의 원자 질량
수소 -2 (중수소) 동위 원소의 원자 질량은 다음과 같이 계산됩니다.
핵의 양성자 수 =1
핵의 중성자 수 =1
수소의 원자 질량 =(1 amu +1 amu)
=2 amu
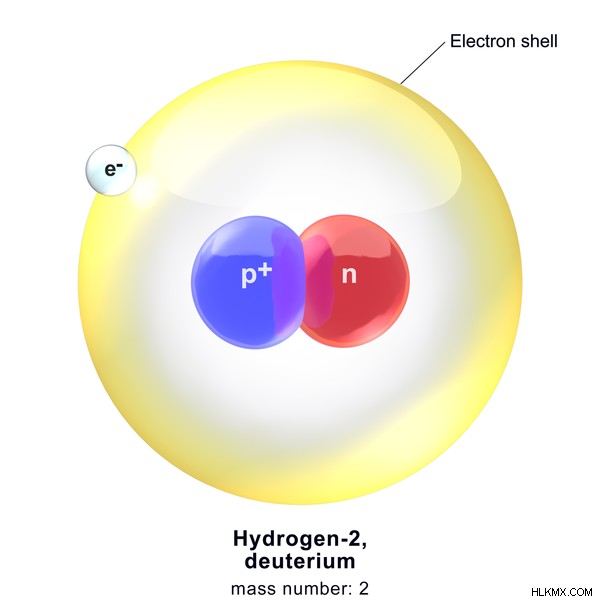
그림 2 :중수소 구조
원자 질량은 단위 AMU (원자 질량 단위)에 의해 주어진다. 하나의 양성자 또는 중성자는 질량이 1 amu입니다.
상대 원자 질량과 원자 질량의 차이
정의
상대 원자 질량 : 상대 원자 질량은 원소의 원자의 평균 질량 사이의 비율입니다.
원자 질량 : 원자 질량은 원자의 핵에 존재하는 핵의 총 질량입니다.
동위 원소
상대 원자 질량 : 상대 원자 질량은 요소의 모든 동위 원소의 질량과 풍부 비율을 사용하여 계산됩니다.
원자 질량 : 원자 질량은 핵 질량을 첨가하여 각각의 동위 원소에 대해 별도로 계산됩니다.
값
상대 원자 질량 : 상대 원자 질량의 값은 Carbon-12 원자의 질량의 12 분의 1에 비해 얻어진다.
원자 질량 : 원자 질량의 값은 직접 계산 된 값 (상대 값이 아님)입니다.
단위
상대 원자 질량 : 상대 원자 질량은 상대 값이기 때문에 치수가 없습니다.
원자 질량 : 원자 질량은 단위 AMU에 의해 주어진다.
결론
원자 질량과 상대 원자 질량은 두 가지 중요한 화학 용어입니다. 비슷하게 들리지만 개념은 다릅니다. 상대 원자 질량과 원자 질량의 주요 차이점은 상대 원자 질량이 원소 원자의 평균 원자 질량의 평균 질량의 평균 질량의 평균 질량과 카본 -12 질량의 1 분의 1의 비율 인 반면 원자 질량은 원자의 핵에 존재하는 핵의 총 질량이다.
.










