결합 된 가스 법칙은 압력, 온도 및 부피 사이의 관계를 정의합니다. Charles 'Law, Boyle's Law 및 Gay-Lussac 's Law를 포함한 세 가지 다른 이름 가스 법에서 파생되었습니다. 아래에서 우리는 법에 대한 방정식, 그것이 어떻게 도출되는지를 설명하고 솔루션과 관련된 연습 문제를 제공합니다.
결합 된 가스 법칙
결합 된 가스 법칙은 다른 모든 것이 일정하게 유지 될 때 (주로 가스의 두더지, n) 압력, 온도 및 부피와 관련이 있습니다. 결합 된 가스 법에 대한 가장 일반적인 형태는 다음과 같습니다.
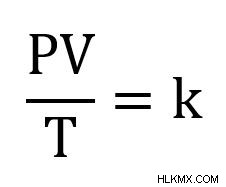
P는 가스의 압력입니다. t는 가스의 온도입니다. V는 가스의 부피입니다. 그리고 K는 일정합니다. k의 정확한 값은 가스 두더지에 따라 다릅니다.
결합 된 가스 법칙은 종종 두 개의 다른 시점으로 작성됩니다. 즉,
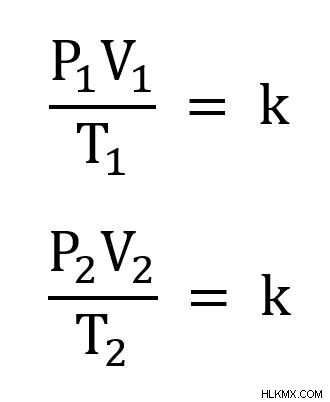
두 K는 동일한 값이므로 서로 동일하게 설정할 수 있습니다. 아래 방정식에서 결과 :
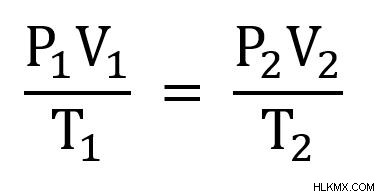
가스 법의 관계는 가스가 이상적인 가스 역할을하는 한 작동합니다. 일반적으로 이것은 온도가 높고 압력이 낮을 때 사실입니다. '이상적인 가스 법'기사에서 가스를 이상적인 가스로 만드는 것에 대해 더 많이 배울 수 있습니다.
결합 된 가스 법률의 파생
결합 된 가스 법은 Charles의 법, Boyle 's Law 및 Gay-Lussac의 법칙을 결합하여 파생됩니다.
Charle의 법칙은 양과 온도 사이의 관계를 제공합니다. 그것은 v/t =k입니다. 보일의 법칙에 따르면 p*v =k라고 말합니다. 그리고 마지막으로, Gay-Lussac의 법칙은 우리에게 p*t =k.
를 알려줍니다
이 모든 관계가 하나의 방정식으로 결합되면 결합 된 가스 법칙을 얻습니다.
결합 된 가스 법칙이 확장되고 가스의 두부가 일정하게 유지되지 않으면 이상적인 가스 법칙을 얻습니다. 또한 이상적인 가스 법칙에서 Backwa를 작업하여 다른 변수를 일정하게 유지하여 다른 가스 법칙을 얻을 수 있습니다. 결합 된 가스 법칙의 경우, 가스의 두부 (N)를 일정하게 유지함으로써 발생합니다.
예제 문제 1
2L의 부피와 760mmHg의 압력이있는 용기에 303K에 가스 샘플이 있다고 가정하십시오. 샘플은 340k의 온도로 이동하고 부피는 2.1l로 약간 증가합니다. 이제 샘플의 압력은 얼마입니까?
솔루션 :
여기서 우리는 두 가지 다른 상태를보고 있습니다. 첨자 1이있는 원래 상태와 첨자 2가있는 두 번째 상태. 먼저 우리가 알고있는 변수를 작성하십시오.
v 1 =2 l
t 1 =303 K
p 1 =760 mmhg
v 2 =2.1 l
t 2 =340 k
p 2 =?
우리는 p 2 를 제외한 모든 변수를 알고 있습니다 . 우리는 또한 우리가 전후 상태를보고 있다고 말할 수 있으므로 다음 방정식을 사용하고 싶습니다.
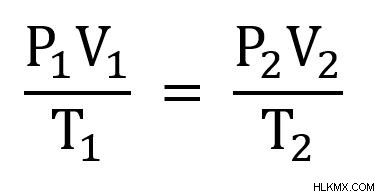
다음으로, 우리는 방정식을 재 배열하여 p 2 를 해결합니다. . 먼저 각면에 t 2 곱하십시오 .
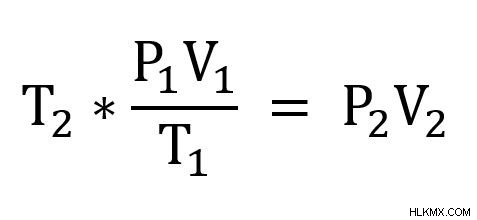
그런 다음 각면을 v 2 별로 나눕니다 .
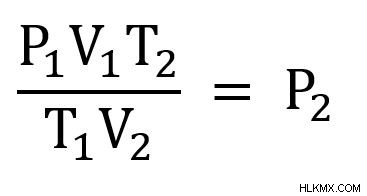
이제 우리는 우리가 알고 해결하는 변수를 연결합니다.
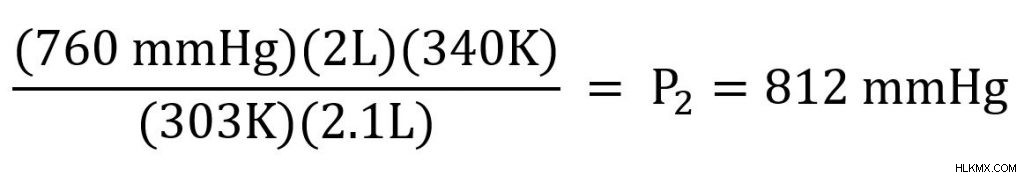
우리의 마지막 압력은 812 mmhg입니다. 또한 압력 장치를 제외한 모든 장치가 취소됩니다.
예제 문제 2
620mmhg 및 177 K에서 가스를 수집합니다. 수집 당시 1.3 L의 부피를 차지합니다. 가스의 부피는 표준 온도와 압력으로 이동할 때 어떻게됩니까?
.솔루션 :
여기서 우리는 가스의 두 가지 상태, 상태 1과 상태 2를보고 있습니다. 따라서 우리는 다음 형태의 결합 된 가스 법을 사용합니다.
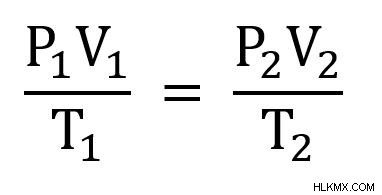
첫 번째 단계는 우리가 알고있는 변수를 결정하는 것입니다. 표준 온도와 압력은 760 mmHg 및 273K로 정의되기 때문에 원래 상태 1에 대한 압력, 온도 및 부피가 원래 상태 1에 대해 주어지고 압력 및 온도는 상태 2에 대해 주어집니다. 우리가 알지 못하는 유일한 변수는 2 권입니다. 이는 우리가 해결해야 할 것입니다.
t 1 =177 K
p 1 =620 mmhg
v 1 =1.3 l
t 2 =273 K
p 2 =760 mmhg
v 2 =?
수학을 더 간단하게 만들려면 v 2 를 해결하기 위해 방정식을 재정렬 해 보겠습니다. 값을 연결하기 전에. 이를 위해, 우리는 양쪽에 t 2 를 곱합니다 그런 다음 p 2 로 나눕니다 .
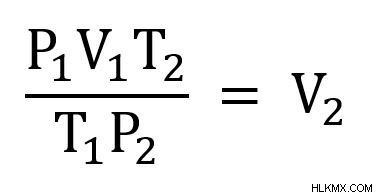
이제 우리는 우리가 알고 해결하는 값을 연결합니다.
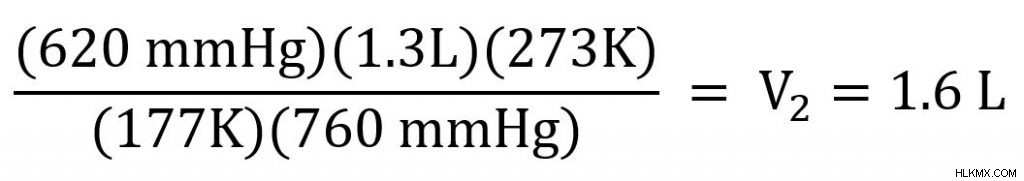
가스의 새로운 부피는 1.6L입니다. 가스의 온도와 압력이 증가함에 따라 가스의 부피도 증가했습니다.
기타 가스 법률
- 찰스 법률
- 보일 법
- Gay-Lussac의 법칙
- 이상적인 가스 법률
- 달튼의 법률
- Avogadro의 법칙
- 헨리의 법칙