핵심 개념
이 유기 화학 튜토리얼에서는 Aldol 응축 반응의 기본 사항, 메커니즘, Enol 중간체 및 Claisen 응축의 기본 사항을 배울 수 있습니다.
다른 기사에서 다루는 주제
- 응축 반응
- 카르 보닐 기능성 그룹
- 친핵체
- electrophiles
- 산 및 염기의 특성
Aldol 응축이란 무엇입니까?
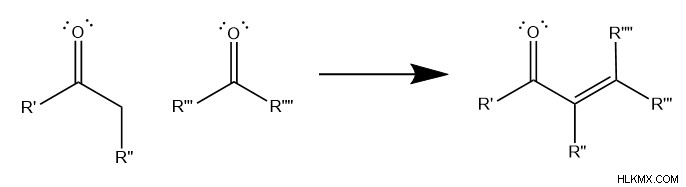
ALDOL 응축은 2 개의 카르 보닐-함유 의 반응을 포함한다 불포화 을 형성하는 분자 두 탄소 사이의 C =C 이중 결합을 갖는 카르 보닐 분자 인접한 아래에 표시된 바와 같이 카르 보닐에. 일반적으로 Aldol 응축은 적어도 하나의 ketone 를 포함해야합니다. , 다른 분자는 ketone 일 수 있습니다. 또는 aldehyde 시작 자료로. 불포화 카르 보닐 생성물의 구조는 반응물 카르 보닐의 구조에 의존한다.
알돌 축합은 다양한 R 그룹에서 발생할 수 있지만, 가장 일반적인 형태의 반응은 메틸 케톤과 알데히드와 관련이 있으며, 이는 불포화 불포화 카르 보닐을 형성하는 알데히드를 포함한다.
.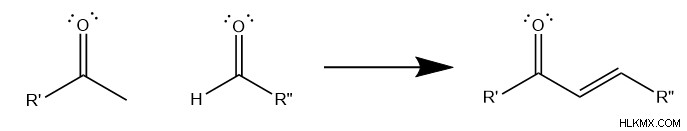
또한 모든 ALDOL 응축은 순 손실 을 초래합니다 2 개의 수소와 하나의 산소. 본질적 으로이 순 손실은 하나의 물 에 해당합니다 분자, 이것이 화학자 들이이 반응을“응축”이라고 부르는 이유입니다.
ENOL 중간체
enol 분자는 중요한 중간체 입니다 알돌 축합에서 다른 많은 유기 반응에 나타납니다. 정의에 따르면, 구조는 c =c double bond 을 포함합니다 (-ENE-) 및 인접한 알코올 (-OL), 화학자들이 Enol (-Ene-plus -ol)이라고 부르는 것을 형성합니다.
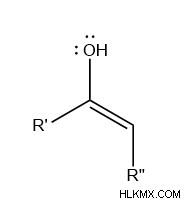
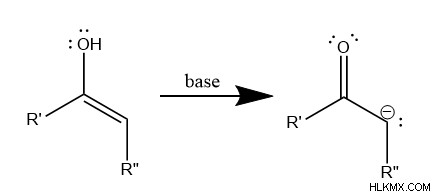
궁극적 으로이 기능 그룹의 조합은 불안정한 경향이 있습니다 , 에놀 그룹에 대한 카르 보닐기의 유리성으로 인해. 결과적으로, 에놀 분자는 빠르게 케토 에놀 타우토머 화를 겪고있다. 기본 또는 중성 조건 하에서, 화학자들이 카르 보닐과 카바이온을 함유 한 에놀 레이트 이온이라고 부르는 것을 형성합니다. 대안 적으로, 산성 조건은 에놀 분자를 다소 안정화 시키지만, 에놀 분자는 특히 반응성이있는 경향이있다.
.
필수 Aldol 응축 메커니즘
흥미롭게도, ALDOL 응축은 산성 또는 기본 조건에서 발생할 수 있지만, 어느 조건 하의 반응 메커니즘은 다릅니다. 두 조건 모두에서, 두 메커니즘은 탈 양성자 을 포함한다 카르 보닐 옆의 탄소 . 이는 카르 보닐의 전자 흡입 효과가 인접한 탄소 수소의 산도를 증가시키기 때문입니다. 두 메커니즘에는 분자 HA와 B가 포함되며, 이는 각각 제네산과 일반적인 염기를 나타냅니다.
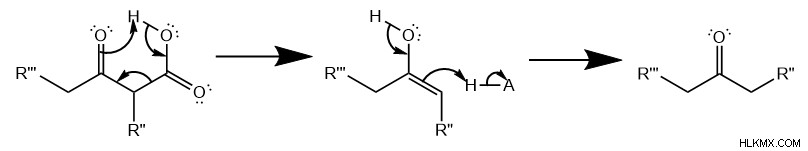
기본 조건 하에서 Aldol 응축
축합 반응을 시작하기 위해, 염기는 제 1 분자의 카르 보닐기 옆에 탄소를 멸치하여 에놀 레이트 분자를 형성한다. 이것은 친 핵성 탄소를 만듭니다 , 탈 양성자화의 결과로 새로 해방 된 전자 쌍으로 인해.
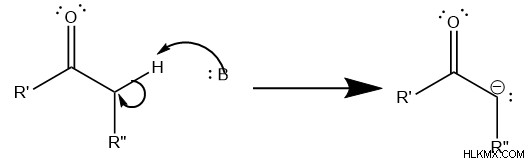
둘째, 친 핵성 탄소 공격 탄소의 두 번째 분자는 산소에 결합되었으며, 이는 산소의 전기성으로 인해 전자 성입니다. 이것은 전자 쌍을 카르 보닐 이중 결합에서 산소로 밀어내어 음이온을 형성합니다. 그러나이 산소는 빠르게 양성자 화되어 알코올을 초래합니다.
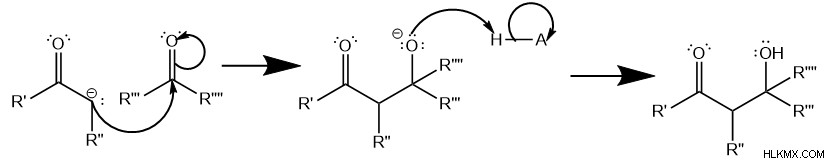
셋째, 제거 반응 산성 탄소가 두 번째로 탈 양성자 화 된 곳에서 발생하여 다른 카바리온 중간체를 형성합니다. 자유 전자 쌍은 알코올을 운반하는 탄소와 이중 결합을 형성하여 알코올을 배출 . 특히, 화학자들은이 단계를 E1CB 반응이라고 부릅니다. (중앙 탄소) 및 상대적으로 가난한 떠나는 그룹 (알코올). "E1"은 그것이 단 분자 제거임을 의미하는 반면 "CB"는 Carbanion Intermediate와 관련된 "Conjugate Base"를 의미합니다.
.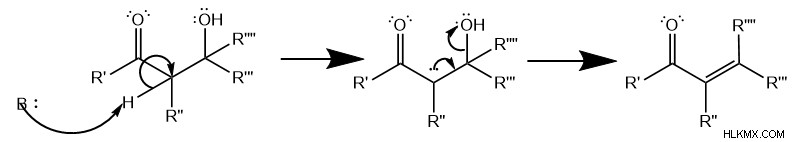
마지막으로, 불포화 카르 보닐 생성물이 형성된다.
산성 조건 하에서 Aldol 응축
시작하기 위해 카르 보닐 제 1 분자의 양성자 인접한 탄소 듀토 톤 입니다 , 에놀 분자 형성.
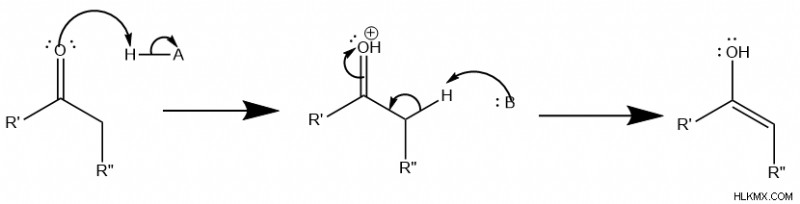
둘째, 이중 결합 에서 하나의 전자 쌍 그런 다음 공격 카르 보닐 두 번째 분자의. 이것은 기본 조건 하에서 메커니즘과 유사하게 빠르게 양자화되는 산소 이온을 형성합니다. 또한,이 친 핵성 공격은 제 1 분자에서 카르 보닐의 개혁을 허용한다.
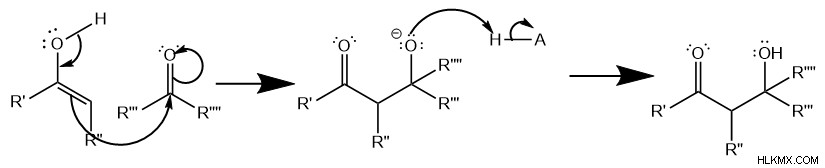
셋째, 제거 반응 발생합니다. 기본 조건과 달리이 단계는 주로 e1 반응 를 통해 진행됩니다. 경로 (적은 양의 E2 반응이 존재할 수 있지만), 이는 강력한 떠나는 그룹 및 탄수화 형성이 포함됩니다. 우선, 새로 형성된 알코올은 두 번째로 양성자 화되어 물 분자의 강력한 잎 그룹을 만듭니다. 물 분자 잎으로 , 탄수화물이 형성되어 중앙 탄소의 수소를 더 산성으로 만듭니다. 이것은 이중 결합 를 형성하는 다른 전자 쌍을 자유롭게하여 두 번째 탈 양성자 화를 허용합니다. .
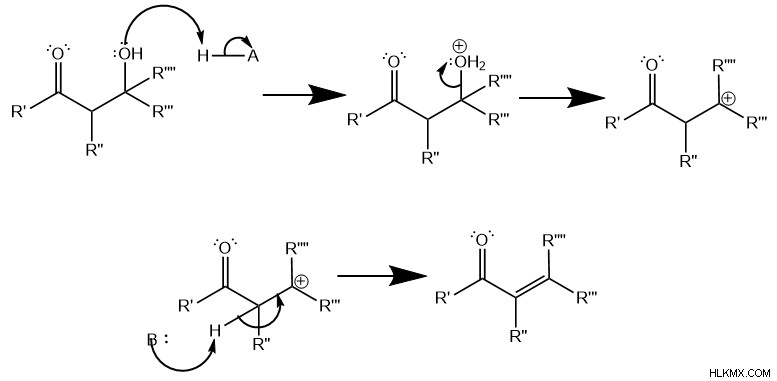
Claisen 응축
중요한 ALDOL 응축 예 중 하나는 claisen 응축 입니다 . 구체적으로,이 반응은 에스테르 를 포함한다 분자 및 베이스 를 따릅니다 조건 메커니즘. 그러나 동일한 알킬 그룹 가있는 카르복시 소금 에스테르는베이스 역할을해야합니다. 이것은 카르 보닐 분자의 카르복시 그룹의 교체를 방지하기위한 것입니다. 또 다른 중요한 차이점은 최종 제품이 디카 보닐 라는 것입니다. 불포화 모노 카르 보닐이 아닌 분자
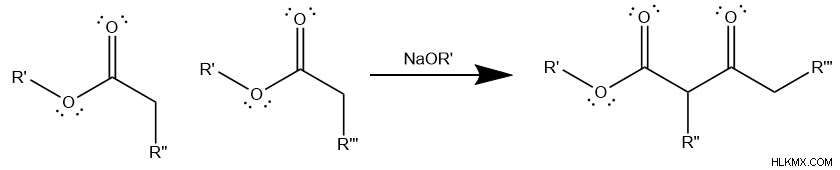
클레이센 응축을 시작하려면 첫 번째 분자의 카르 보닐 옆에있는 탄소는 탈포 톤 입니다. . 그 결과 카바리온은 공격 전자성 카르 보닐 탄소 두 번째 분자의. 결과적으로 C =O 채권 개혁은 카르복시 그룹을 배출하는 를 배출합니다 .
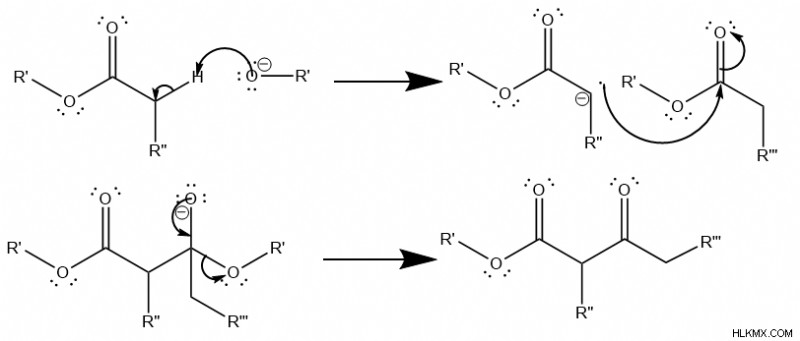
다음으로, 물 에서 클레이센 응축이 발생하는 경우 , 그런 다음 알코올 그룹은 나머지 ester 을 대체합니다 그룹. 이로 인해 카르 복실 산 그룹이 발생합니다.
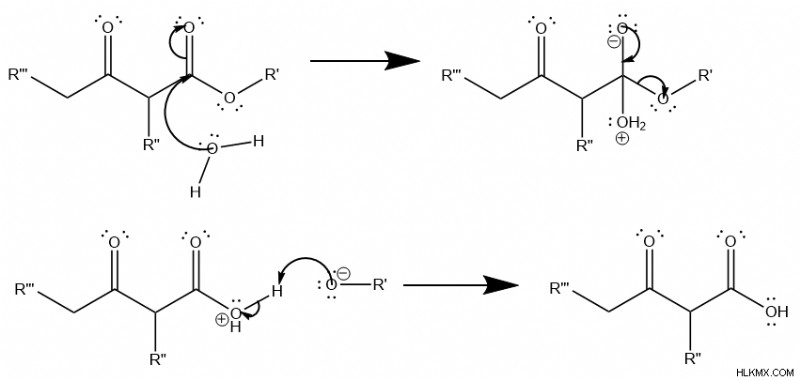
그러나,이 카르 복실 산 분자는 안정성이 부족하고 고온에서 분해됩니다. 구체적으로, 데카르 복실화 절단 인 전자의 원형 이동을 포함합니다 카르 복실 산은 이산화탄소를 방출합니다 . 생성 된 에놀 분자는 ketone 으로 동형 화된다 . 데카르 복실화는 많은 중요한 생물학적 경로, 특히 구연산주기에서 발생합니다.