핵심 개념
이 튜토리얼에서는 떠나는 그룹 를 배울 것입니다. 좋은 것을 식별하는 방법뿐만 아니라. 또한 다른 유기 화학 반응에서 볼 수있는 떠나는 그룹의 예 목록을 배웁니다.
다른 기사에서 다루는 주제
- 친핵체
- electrophiles
- 양이온 및 음이온
- 산 및 염기의 특성
- PKA
- 공명
- 응축 반응
어휘
- 음이온- 음으로 하전 된 이온
- 기본성- 분자가베이스 역할을하는 방법
- 양이온- 긍정적으로 하전 된 이온
- conjugate base- 산이 산성 수소를 잃을 때 형성된 분자
- 공명- 다른 전하 위치를 만들기 위해 분자의 인접한 장소로 이동하는 전자
그룹 정의 떠나
떠나는 그룹은 고독한 쌍을 갖는 분자에서 벗어날 수있는 원자 또는 원자 그룹으로, 그것과 분자 사이의 결합을 깨뜨린다. 그것은 친핵체의 반대 역할을한다. 공유 결합을 형성하기 위해 전자를 기증하는 대신, 그 결합을 깨고 전자가 떠날 때 전자를 취합니다. 이 때문에 주요 분자는 일반적으로 누락 된 전자가 남아 양이온이됩니다.
떠나는 그룹은 일반적으로 음이온 또는 중립이지만 양이온이 될 수 있습니다.
좋은 떠나는 그룹을 만드는 것은 무엇입니까?
원자 또는 원자 그룹이 자체적으로 안정적 일수록 잎 그룹이 더 좋습니다.
약한베이스
좋은 떠나는 그룹은 강산의 접합체 인 약한 염기입니다. 고독한 쌍의 컨쥬 게이트베이스가 더 안정적 일수록베이스가 약할 것입니다. PKA는 안정적인 고독한 전자 쌍의 전자 쌍의 측정으로 사용될 수 있습니다. PKA가 낮을수록 산이 강하고 접합체베이스가 약해집니다. 여기에서 자세히 알아보십시오.
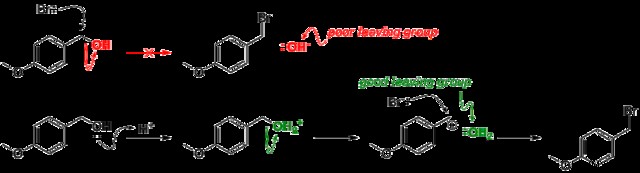
크기 대 기본성
우리가 주기성 테이블의 오른쪽으로 이동하면 크기가 증가합니다. 크기와 염기성은 반대 관계를 갖습니다. 이는 크기가 증가함에 따라 염기성이 감소함에 따라 의미가 있습니다. 따라서 잎 그룹의 크기가 클수록 기초로 약하고 분자에서 벗어날 가능성이 높아집니다.
공명
공명은 분자의 안정성에 큰 역할을한다. 분자 내의 전자의 움직임에 의해 전하가 재배치되거나 중화 될 수있는 시점이다. 약한 염기는 일반적으로 단독으로 견딜 수있을 정도로 안정적 인 공명 구조를 가지고 있습니다. 따라서 퇴근 그룹이 공명 안정화 될 수 있다면 주 분자에서 쉽게 벗어날 가능성이 더 높습니다.
그룹 예제
- Halides- Br, I, Cl
- 설폰 네이트- 오트, oms
- 암모니아 nh3
- Water-H 2 o
추가 읽기
- E1 반응
- E2 반응
- SN1 반응
- SN2 반응