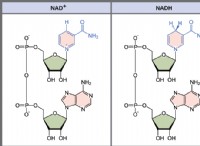
탄화수소는 두 가지 주요 원자로 구성된 유기 화합물로 설명 될 수 있습니다. 여기에는 탄소와 수소가 포함됩니다. 일반적으로 이들은 냄새가 거의없는 무색 가스입니다. 유형에 따라 탄화수소는 단순하거나 복잡한 구조를 가질 수 있습니다. 이것들은 알켄, 알칸, 알킨스 및 아로마의 네 가지 주요 부분으로 분류됩니다.
탄화수소를 이해함으로써, 우리는 여러 중요한 유기 화합물, 기능 그룹 및 제제의 화학적 특성을 조사 할 수 있습니다. 오늘날, 우리는 탄화수소와 다른 사람들의 준비에 대해 자세히 읽을 것입니다. 더 이상 고민하지 않고 시작합시다!
탄화수소는 무엇입니까?
탄화수소는 수소와 탄소라고 불리는 필수 원자로 구성된 유기 화합물에 속합니다. 일상 생활에서 탄화수소는 중요한 역할을하며 그들의 연구는 기능 그룹의 특성과 준비에 대한 깊은 통찰력을 제공합니다.
탄화수소는 주로 6 가지 범주로 나뉩니다. 여기에는 포화 탄화수소, 불포화 탄화수소, 사이클로 알칸, 방향족 탄화수소, 지방족 탄화수소 및 알리시 클릭 탄화수소가 포함됩니다.
프로판 및 부탄과 같은 여러 탄화수소는 LPG 또는 액화 석유 가스와 같은 상업적인 연료 목적으로 사용됩니다. 또 다른 중요한 방향족 탄화수소 인 벤젠은 합성 약물을 만드는 원료입니다. 카로틴이라는 또 다른 탄화수소는 당근에서 일반적으로 발견되는 유기 안료입니다.
알켄은 무엇입니까?
알켄은 탄화수소 제품군에서 나옵니다. 알켄은 적어도 두 개의 인접한 탄소 원자 (알켄 CNH2N의 화학적 공식) 사이에 단일 이중 결합을 갖는다. 알켄을 준비 할 수있는 몇 가지 방법이 있습니다. 가장 인기있는 방법 중 일부는 여기에서 논의됩니다.
알켄의 일반적인 특성 :
여기 알켄의 몇 가지 일반적인 속성이 있습니다 :
-
물리적 상태 - 알켄에서 2 ~ 4 개의 탄소 원자를 가진 부재를 가스라고합니다. 5-17은 액체라고하며, 18+는 실온에서 고체로 알려져 있습니다. 또한, 알켄은 공중에서 화상을 입고 연기가 자욱한 불꽃을 형성합니다.
-
용해도 - 알켄은 유기 용매에 용해되는 반면, 물에 불용성이 있습니다. 몇 가지 예는 벤젠 등입니다.
-
밀도 - 물보다 가볍습니다.
-
끓는점 - 체인 길이 또는 분자 질량이 증가함에 따라 알켄의 끓는점도 증가합니다. 분자간 명소는 분자 크기가 증가함에 따라 강도를 얻는 경향이 있음을 보여줍니다.
탄화수소 준비 - 실험실의 알켄
Alkynes의 Alkenes :
Alkenes를 준비하려면 Alkynes가 상당히 자주 사용됩니다. 알키네에서 알켄 전환은 일반적이며, 팔라드 화 된 숯이있을 때 수소로 알킨을 감소시킴으로써 수행된다.
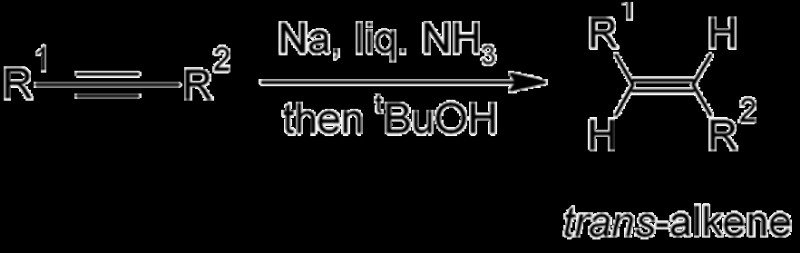
공정에 사용 된 숯은 궁극적으로 알켄을 형성하는 황과 퀴놀린 화합물을 통해 적당히 비활성화됩니다. 상기 반응으로부터 달성 된 알켄은 시스 형상을 갖는다. 알키네스는 액체 암모니아의 나트륨으로 환원 과정을 겪고 트랜스 알켄을 형성한다.
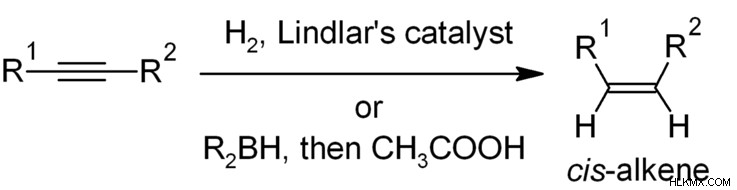
알킬 할라이드의 알켄 :
알킬 할라이드가 알코올 칼륨으로 가열되면 알켄이 얻어진다. 알코올 칼륨은 수산화 칼륨이 알코올에 용해 될 때 달성됩니다. 여기서, 탈히 할로겐화가 발생하며, 이는 할로겐 산의 단일 분자가 제거됨을 의미한다. 반응 속도는 대부분 알킬기에 의존합니다. 그러나 할로겐 그룹의 성격이 붙어 있습니다.
여기 Alkyl Halides의 알켄 준비가 있습니다 :
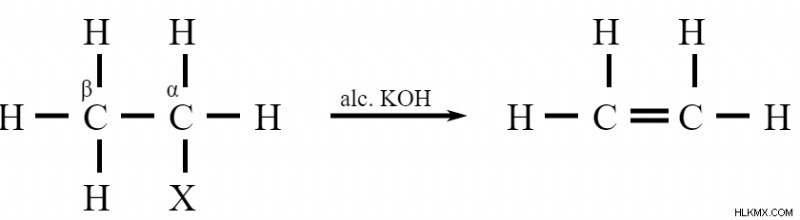
여기서 x는 cl, br 또는 i입니다.
Vicinal Dihalides의 알켄 :
Vicinal Halides는 2 개의 인접한 탄소 원자가 2 개의 할로겐과 밀접하게 연결된 디하라 드입니다. 이러한 디 하이드가 아연 금속과 직접 접촉 할 때마다 할로겐 분자가 손실되어 알켄을 형성합니다. Dihalides Vicinal Dihalides로부터의 알켄의 형성을 탈할 로겐으로 지칭된다.
여기에 vicinal dihalides의 알켄 준비가 있습니다 :
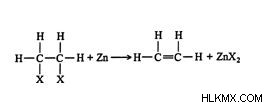
알코올로부터의 알켄 :
알코올이 농축 황산과 접촉 할 때 물 분자의 제거로 인해 알켄을 형성합니다. 여기에는 물 분자가 없기 때문에 알코올의 산성 탈수라고합니다. 여기서 황산은 탈수 제입니다.
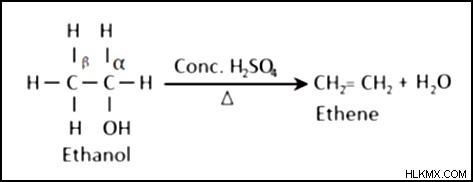
알켄의 사용 :
다음은 프로 펜, 에텐 등과 같은 알켄의 용도입니다.
를 살펴 보겠습니다.-
폴리에틸렌과 같은 플라스틱 제조에 사용하여 버킷, 가방, 그릇 등을 제조합니다.
-
폴리스티렌 제조에 사용되는 냉장고 부품, 자동차 배터리 등을 만드는 데 사용됩니다.
-
자동차 라디에이터에 사용하기 위해 Ethane-1,2-Diol을 만드는 데 사용됩니다.
-
합성 섬유 Terylene 및 에탄올을 만드는 데 사용됩니다.
-
반 옥시를 만드는 데 사용됩니다.
-
포장재와 로프를 생산하기 위해 플라스틱을 만드는 데 사용됩니다.
-
아크릴 섬유를 만드는 데 사용됩니다.
알칸은 무엇입니까?
알칸은 단일 결합 수소 및 탄소 화합물을 갖는 유기 화합물로 설명 될 수있다. CNH2N+2는 알칸의 공식입니다. 사이클로 알칸, 분지 알칸 및 체인 알칸의 세 가지 주요 그룹으로 나뉩니다.
|
molecular gormula. | |
|
| |
|
|
|
|
(c3h8 | |
|
| |
|
| |
|
| |
|
| |
|
| |
|
|
|
|
|
|