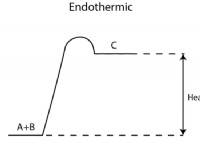
좌표 화합물은 좌표 또는 dative 결합을 통해 리간드로 둘러싸인 중앙 금속 원자를 갖는다. 이 경우, 중앙 금속은 루이스 산으로 기능하며 루이스 염기로서 기능하는 리간드에서 전자를 받아들입니다. Alfred Werner는 조정 화합물에 대한 그의 관점을 최초로 제공했습니다. 이 화합물은 결정 격자 및 용액 또는 용융 상태에서 동일성을 유지합니다.
[NI (NH3) 6] 2+는 니켈이 중심 금속 원자 역할을하는 잘 알려진 예이며, 암모니아는 리간드 역할을합니다.
조정 다면체는 무엇입니까?
'조정 다면체'라는 용어는 중심 원자 또는 이온에 직접 연결된 리간드의 기하학적 패턴 또는 공간 배열을 설명합니다.
- 가장 빈번한 배위 다면체는 사면체, 팔면체 및 정사각형 평면 형상입니다.
예 :
- [ni (Co) 4]의 기하학은 사면체입니다
- [Ni (CN) 4] 2-의 기하학은 제곱 평면 입니다
- [Fe (Co) 5]의 기하학은 삼각형 비 피라미드 입니다
- [pt (cl6)] 2-의 기하학은 팔면체 입니다
- Werner에 따르면 1 차 및 2 차 원자가는 조정 화합물에서 발견되는 두 가지 유형의 원자가입니다.
1 차 원자가 :
점선은 1 차 원자가의 복합체에 대한 산화 상태 또는 전하를 나타내며, 이는 전환 가능하다.
2 차 원자가 :
2 차 원자가는 불가능하며 실선으로 표시됩니다. 그것은 분자의 형상 또는 형태를 결정합니다.
- 1 차 원자가는 비 방향이며 2 차 원자가는 방향입니다.
1. [NI (NH3) 6] CL2 :
- 실선 (2 차 원자가)은 암모니아를 나타내며 점선은 염소 (1 차 원자가)를 나타냅니다. 조정 개체 또는 복합체는 정사각형 괄호 안에있는 종이며, 카운터 이온은 정사각형 브래킷 외부의 종입니다.
- 1st, 2nd 또는 3rd 기간 전이 요소는 일반적으로 중앙 금속 원자로 사용됩니다. 고독한 쌍 또는 기증 할 음전하가있는 모든 분자는 리간드로 사용될 수 있습니다.
2. 모노 덴테이트 리간드-
단일 분열 리간드, 암모니아 (NH3), 카르 보닐 (CO) 및 포스 핀 (PH3) 그룹에 하나의 공여자 부위만이 존재한다.
-
비 지체 리간드-
리간드에는 2 도구 부위가 있습니다. 옥살 레이트 (C2O4) 2-는 좋은 예입니다.
-
폴리 덴테이트 리간드-
2 개 이상의 공여자 원자가 다 첨가 리간드에 존재한다. EDTA (에틸렌 디아민 테트라 아세테이트)는 육각형 리간드의 예입니다.
- 리간드는 일반적으로 공여자입니다. 그러나, PI 산 리간드 및 PI 염기 금속으로도 알려진 분자 궤도 또는 빈 D 궤도에서의 PI 결합은 리간드가 금속으로부터 전자를 흡수 할 수있게한다.
- 동종 및 이종 복합체는 두 가지 유형의 복합체입니다. 동일한 유형의 리간드로 둘러싸인 금속은 동종성으로 간주되는 반면, 2 가지 이상의 리간드로 둘러싸인 금속은 이질적인 것으로 간주됩니다.
형태에 기초한 폴리 헤드론의 유형
- 사면체
- 제곱 평면도
- 삼각형 Bipyramidal
- 팔면체
- 2에서 16 사이의 조정 번호는 일반적으로 6이면 중심 요소에 대한 총 부착 지점 수입니다. 간단히 말해, 금속 이온의 전자 구성에 의존하는 금속 이온과 리간드 및 전자 요인의 상대 크기 및 전자 요인은 복합체의 조정 번호를 결정합니다.
- 반경 비율에 따르면, 중앙 이온의 전하가 높을수록 음으로 하전 된 리간드에 대한 인력이 더 커집니다. 그러나 전하가 클수록 이온이 작아지면 조정할 수있는 그룹의 수가 제한됩니다. 모든 지오메트리는 고유 한 조정 번호가 있지만 해당 숫자를 가진 모든 단지는 다양한 형상을 선택할 수 있다는 것을 기억하는 것이 중요합니다.
조정 번호 3
- Trigonal Planar Geometry :Co32-와 같은 주요 그룹 종에 잘 알려진이 지오메트리는 리간드 결합 각도가 120 도의 평면에 4 개의 원자를 포함합니다.
조정 번호 4
두 가지 가능한 형상이 있습니다. 사면체는 더 일반적이지만 정사각형 평면은 D8 전자 구조를 갖는 금속 이온과 거의 독점적으로 연관되어 있습니다.
- 사면체 기하학 :유기 화학 과정은 사면체 C 원자를 중심으로 한 분자의 화학을 검사합니다. 사면체 코발트 (II) 복합체는 막대한 수로 존재한다.
- 정사각형 평면 형상 :이것은 몇 가지 중요한 화합물을 함유하고 있기 때문에 언급 된 상당히 드문 모양입니다.
조정 번호 5
- 사각형 피라미드 형태는 VO (ACAC)와 같은 옥소 바나듐 염 (Vanadyl, VO2+)에서 일반적입니다. 특히, 바나듐 (IV)은 좌표 적으로 불포화되어 피리딘이 첨가 될 때 팔면체의 생산을 초래한다.
- 1968 년 [CR (en) 3] [Ni (CN) 5] 1.5 H2O의 구조는 동일한 결정에서 두 가지 유형의 기하학을 보여주는 복합체의 놀라운 예로 설명되었습니다.
결론
배위 화합물은 고체 및 액체 상태에서 동일성을 유지하는 분자 첨가 화합물이다. 이들 화합물의 중앙 금속 원자 또는 이온은 이온 또는 분자에 의해 좌표 결합과 연결된다.
- 예를 들어,
- 페로 시안 칼륨의 경우 K4 [Fe (CN) 6].